-
任何昆虫的行为都具有周期性的节律特征[1], 因此, 掌握昆虫行为活动节律, 有利于更好地开展害虫防治或益虫保护工作。然而, 目前关于蝴蝶成虫行为的系统研究较少, 仅王翻艳等[2]和Li等[3]分别对观赏蝴种大帛斑蝶(Idea leuconoe(Erichson))和青斑蝶(Tirumala limniace(Cramer))成虫的飞行、访花、求偶、交配和产卵行为作了系统观察。其余关于蝶类成虫行为的研究国内主要围绕一些濒危或保护蝶种的取食、交配或产卵等部分行为展开, 以期通过对行为的研究找出影响其繁殖的因素或野生种群保护的措施[4-7]。国外则侧重于从化学生态学角度寻找吸引蝴蝶取食[8-11]、交配[12-13]或产卵的化合物[14-15]以及研究对蝴蝶种群繁衍至关重要的产卵行为[16]。
金斑蝶(Danaus chrysippus(Linnaeus))为鳞翅目(Lepidoptera)斑蝶科(Danaidae)斑蝶属(Danaus Kluk), 国内分布于海南、云南、广东、广西、福建、台湾、四川、江西、湖北和陕西等地[17]。成虫喜访马利筋, 性情温和, 飞行低缓, 姿态优雅, 非常适应人工繁殖园内小生境。对经济和园林植物无害, 是集工艺、生态观赏和喜庆放飞三用蝶种, 具较高的开发利用价值, 在南方各地广为养殖。在云南元江地区, 1年可发生10代以上[18]。
在金斑蝶的行为方面, 王文明[7]研究了燕山地区金斑蝶的生物学特征, 并对其交尾节律和产卵行为做了详细观察, 发现6—7月为其适宜的繁殖月份。Tang等[19]通过对金斑蝶访花行为选择发现, 其在访花过程中, 以视觉信号为主, 嗅觉信号为辅; 但关于金斑蝶成虫行为学研究还未见系统报道。作为优良的三用蝶种, 系统地观察金斑蝶成虫的飞行、取食、交配和产卵行为, 不仅可掌握其成虫的活动特点与规律, 了解成虫的生物学习性, 还可对金斑蝶的人工规模化繁育及野生种群的保护提供理论支撑, 并为金斑蝶飞舞景观营造提供理论依据。
-
供试蝴蝶为人工养殖的临近羽化的金斑蝶蛹。蜜源植物为马利筋。
-
中国云南元江县干热河谷区中国林业科学研究院资源昆虫研究所试验站, 海拔约400 m, 实验在网室内(4 m×8 m×4 m)进行。网室透光良好, 光照均匀。
-
参照周成理[5]对枯叶蛱蝶成虫习性的观察方法和Li等[3]对青斑蝶成虫行为的研究方法, 于6月中旬每日6:30—19:00在田间的网室内持续观察金斑蝶成虫的羽化、飞行、取食、求偶、交配和产卵行为, 并记载其羽化、飞行和取食时间。
-
将挂有临近羽化的金斑蝶蛹的塑料盆放入网室内的支架上。次日早晨成虫羽化前(6:30)开始观察记录成虫的羽化时间。
-
待新羽化成虫翅膀基本硬化(约羽化后40 min), 用油性记号笔标记雌雄各10头, 以其中1~3号雄虫, 4~6号雌虫作为初始观察对象, 跟踪观察其日飞行的起始时间。
-
跟踪观察标记成虫的日取食起始时间及其取食行为。
-
跟踪观察标记成虫的交配起始时间及其求偶和交配行为。
-
跟踪观察标记成虫的产卵行为以及产卵地点和方式。
同时通过摄像机记录其余放飞的金斑蝶, 作为行为分析的补充。网室中央集中摆放处于盛花期的马利筋盆栽16盆。
-
采用SPSS23.0统计分析软件对数据进行单因素方差分析和相关分析。
-
金斑蝶羽化时, 首先是蛹体背部裂开, 然后成虫的胸足慢慢从裂口伸出, 逐渐爬出蛹壳, 接着用足抓住蛹壳, 倒挂身体。随着身体的倒挂, 翅膀由皱缩不断变大变硬, 并伴有数滴黑褐色液体—蛹便从腹部排出。约10 min后翅膀完全舒展开, 但成虫不立即飞行, 而是在原处抖动拍打翅膀或向上爬行。供试金斑蝶成虫羽化均在上午完成, 最早羽化时间为6:46, 主要集中在8:00—10:00。雄蝶羽化时间早于雌蝶, 但在羽化时间分布上雌蝶更为集中。
表 1 金斑蝶羽化时间
Table 1. The eclosion time of Danaus chrysippus
雄蝶Male 雌蝶Female 编号No. 羽化时间Eclosion time 编号No. 羽化时间Eclosion time 1 6:46:00 4 7:53:19 2 7:25:36 5 7:57:52 3 8:40:01 6 9:48:18 7 9:26:04 10 8:14:34 8 9:30:54 11 8:33:54 9 8:44:20 12 8:51:25 13 9:16:15 16 8:52:13 14 9:09:59 17 9:47:36 15 9:16:15 18 10:36:01 19 9:50:02 20 10:22:40 21 7:36:49 29 8:18:07 22 8:10:10 30 8:21:40 23 8:48:20 31 8:45:54 24 8:58:58 32 8:50:47 25 9:03:02 33 9:05:14 26 9:05:20 34 9:16:53 27 9:09:59 35 9:38:11 28 9:6:15 36 9:40:46 -
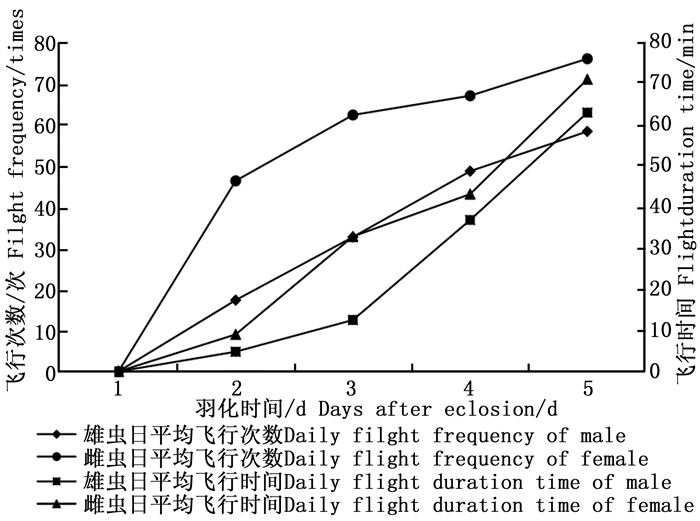
成虫羽化当天基本处于停歇状态, 偶有几次转换停歇位置在网室壁上的爬行行为。自羽化第2天起, 雌雄成虫的日平均飞行次数及日平均飞行时间均逐渐增加(图 1)。金斑蝶的雌雄成虫在7:00之前就开始少量的飞行活动, 雄成虫的日飞行高峰在13:00—15:00, 雌成虫的日飞行高峰为9:00—11:00和15:00—17:00(图 2)。金斑蝶在羽化后至产卵前, 雌虫飞行总次数为176次, 飞行总时间为84.90 min, 平均每天飞行44次, 飞行21.23 min, 单次平均飞行时间0.48 min; 雄虫的飞行总次数为99次, 飞行总时间为54.10 min, 平均每天飞行25次, 飞行13.53 min, 单次平均飞行时间0.54 min。雌雄成虫的日平均飞行次数、平均飞行时间和日飞行规律均无显著差异(p > 0.05);飞行次数与飞行时间均呈显著正相关(雌蝶: r=0.978, p < 0.05;雄蝶: r=0.957, p < 0.05)。
-
观察发现, 金斑蝶雌雄成虫羽化当日均不取食, 次日才开始取食。自羽化第2天起, 雌雄成虫的日平均取食次数及日平均取食时间均逐渐增加(图 3)。

图 3 雌雄成虫羽化后至产卵前的日取食次数与时间
Figure 3. The daily feeding frequency and duration time of female and male from eclosion to oviposition
金斑蝶接近7:00开始取食活动, 之后取食次数逐渐增多, 交配前, 雄虫的日取食活动有一个高峰期在9:00—11:00, 之后取食次数下降; 雌虫有2个取食高峰期, 分别在11:00—13:00和15:00—17:00, 17:00后取食次数逐渐减少, 直至停止活动(图 4)。

图 4 雌雄成虫羽化后至产卵前的日取食节律
Figure 4. The daily feeding rhythm of female and male from eclosion to oviposition
金斑蝶在羽化后至产卵前, 雌虫的取食总次数为134次, 取食总时间为343.00 min, 平均每天取食34次, 取食85.75 min, 单次平均取食时间2.52 min; 雄虫的取食总次数为85次, 取食总时间为293.00 min, 平均每天取食21次, 取食73.25 min, 单次平均取食时间3.49 min。
雌雄成虫的日平均取食次数、平均取食时间和日取食规律均无显著差异(p > 0.05);取食次数与取食时间均无显著正相关(雌蝶: r= 0.949, p > 0.05;雄蝶: r=0.853, p > 0.05)。
-
金斑蝶雄成虫的交配求偶属于巡游型, 雄成虫在网室内巡回飞行, 主动寻找雌成虫交配, 当遇到有交配意愿的雌成虫时, 双双在空中漫游, 然后雌成虫停落在网室壁、地面或植物枝叶上, 紧接着雄成虫也停落在雌成虫旁并将腹部伸出弯曲至雌成虫腹末开始交配。
最早交配时间发生在羽化第4天。雌雄成虫均可多次交配, 交配主要发生在14:00—16:00;最早交配开始于11:03, 止于16:00—17:00, 最晚开始于17:56, 过夜后于次日6:30前结束。在观察到的4对成虫共7次交配时间中, 交配持续时间最短16 min, 最长357 min, 平均交配时间(174.71±152.07) min。
大多数雌成虫交配次日便开始产卵, 也有个别雌成虫交配当天即开始产卵。产卵时, 雌成虫搜寻到产卵地后首先停落在要产卵的部位上, 然后用腹部接触摩擦几次产卵部位, 最后将腹部弯曲, 产出卵1枚。产卵最早开始于8:31, 最晚止于18:12, 产卵时间主要在11:00—13:00。金斑蝶雌成虫的产卵方式为散产, 主要产卵于寄主植物叶片背面, 其次为茎杆, 少数产于寄主植物花朵、寄主植物叶片正面、杂草和花盆上。
-
蝶类成虫经过羽化后才具备飞行能力, 目前蝶类的羽化节律已有较多报道, 且结果表明不同种类之间的羽化时间有差异, 多数发生在4:00—6:00和上午[20-24]。本研究中, 金斑蝶最早羽化时间为6:46, 主要集中在8:00—10:00, 与王文明[7]对燕山地区金斑蝶的羽化节律相吻合; 在羽化时间上, 雄蝶羽化时间早于雌蝶, 这也符合在外界条件相同的情况下, 雄蝶比雌蝶先羽化的研究结果[20, 23, 25-26]。金斑蝶与枯叶蛱蝶、大帛斑蝶和青斑蝶一样[2-3, 5], 羽化当天基本不活动, 为停歇状态, 说明其处于运动器官成熟阶段。通过飞行肌的锻炼, 待其发育成熟后为飞行做准备[27]。
飞行是蝶类开展其他活动的前提, 金斑蝶也不例外, 其成虫的飞行活动与取食、交配和产卵等行为密切相连, 不取食、交配或产卵时, 成虫基本都处于停歇状态。蝴蝶为变温动物, 通过外界温度调节蝴蝶飞行期身体的温度影响其飞行能力[8], 从而影响其在飞行、繁殖、休息、取食的时间分配[28]。蝴蝶在阴雨天一般停止飞行[29]。金斑蝶的雌雄成虫在7:00之前就开始少量的飞行活动, 雄成虫的日飞行高峰在13:00—15:00, 雌成虫的日飞行高峰期为9:00—11:00和15:00—17:00。四川绢蝶(Parnassiida szechenyii(Frivaldszk))10点开始有少量活动, 12:00—13:00达到高峰[29]; 曲纹紫灰蝶(Chilades pandava(Horsfield))7:30开始少量活动, 9:30—10:30达到日活动高峰[30]。夏季, 枯叶蛱蝶(Kallima inachus(Doyére))大多在11:00—13:00和15:00—17:00活动[5]。说明不同蝶种、不同性别和不同环境温度都可以对蝴蝶的飞行产生影响[31]。
昆虫的访花活动节律主要受环境温度、昆虫自身的生理特征、蜜源植物等多种因素的影响, 因此, 不同蝴蝶的访花时间和访花高峰期有所差异[29, 32]。本研究中, 从羽化后到交配前金斑蝶的取食次数逐渐增加, 与大帛斑蝶和青斑蝶类似[2-3], 说明其同样处于补充营养和促进生殖器官发育阶段。通过补充营养不仅能促进生殖系统的发育成熟, 还能为日常生命活动提供活动能量以及延长成虫的产卵期, 对于蝴蝶生殖具有重要意义[33-34]。
蝴蝶的求偶有2种类型: 巡游型和等候型[18]。金斑蝶与大帛斑蝶、青斑蝶、四川绢蝶[2-3, 8]都属于巡游型, 枯叶蛱蝶为等候型[5], 说明不同蝶种的求偶方式有差异, 巡游型主要见于凤蝶科和粉蝶科[18]。王文明[7]对燕山地区金斑蝶的生物学研究表明, 交配发生在10:00—16:00, 时长(94.6±22.39) min, 交配后雌虫将大部分卵散产于寄主植物叶背面。在元江地区, 金斑蝶的羽化规律、产卵方式和产卵部位与燕山地区相同, 但成虫交配发生在14:00—16:00, 平均交配时间为(174.71±152.07) min, 这可能与元江的气温较燕山地区高, 蝴蝶成虫活动受温度影响有关。一旦出现求偶和交配行为, 成虫即进入求偶和交配阶段。
交配完成后, 成虫进入产卵阶段。多数情况下, 蝴蝶将卵主要产于寄主植物的嫩叶嫩梢的背面, 有利于减少卵受日晒、雨淋以及天敌的侵害[35], 如玉带凤蝶(Papilio polytes(Linnaeus))、青斑蝶、大帛斑蝶[2-3, 24], 有的种类则喜产卵在寄主植物附近或寄主植物叶片正面, 如枯叶峡蝶[5]。雌蝶的产卵方式因蝶种不同有所差异, 金斑喙凤蝶(Teinopalpus aureus(Mell))、青斑蝶、大帛斑蝶、枯叶蛱蝶等为散产, 丝带凤蝶(Sericinus montelus(Gray))、红锯蛱蝶(Cethosia biblis(Drury))、白带锯蛱蝶(C. cyane(Drury))和文蛱蝶(Vindula erota(Fabricius))等为聚产[18]。散产可有效避免后代对食物的竞争, 聚产则可发挥集体防御功能。因此, 不管何种产卵方式, 均是成虫为使后代成功繁衍所采取的适应性措施。
-
金斑蝶在成虫期的行为特征与同为斑蝶科的大帛斑蝶和青斑蝶有类似规律, 说明斑蝶科蝴蝶成虫活动规律有一定的共性。因此, 同样可将其成虫期归纳为4个阶段: 运动器官成熟阶段、补充营养和促进生殖器官发育阶段、求偶和交配阶段、产卵阶段, 各阶段内行为有交叉[2]。运动器官成熟阶段从羽化当天开始到成虫出现求偶交配行为为止, 一般历时4~5 d; 补充营养和促进生殖器官发育阶段历时时间最长, 从羽化第2天一直持续到成虫死亡; 求偶交配阶段和产卵阶段的持续时间则与成虫的交配次数有关, 交配次数越多, 产卵次数越多, 每交配1次可持续产卵3~6 d。
在掌握其成虫行为特征后, 为更好地在蝴蝶生态园中观赏到金斑蝶飞舞景观, 可在园内释放羽化2~3 d后的成虫, 同时尽量选择金斑蝶飞行和取食的高峰时间段对外开放。下一步还可以根据行为研究的理论指导, 充分结合温度、光照等环境因子, 通过对金斑蝶蜜源植物、寄主植物和成虫性信息素中挥发物的鉴定, 通过田间实验找出吸引其取食、产卵和交配行为的关键化合物, 达到人工调控行为, 营造更绚丽缤纷的蝴蝶飞舞景观效果。
金斑蝶成虫行为学特征
Adult Behavior Feature of Danaus chrysippus
-
摘要:
目的 为摸清金斑蝶成虫的行为特征, 方法 在田间的网室内跟踪观察其飞行、取食、求偶、交配和产卵行为。 结果 表明:金斑蝶成虫羽化主要集中在8:00—10:00,成虫羽化当天基本处于停歇状态;羽化第2天起至交配前,雌雄成虫的日平均飞行次数及日平均飞行时间均逐渐增加,雄成虫的日飞行高峰在13:00—15:00,雌成虫的日飞行高峰期在9:00—11:00和15:00—17:00,雌雄成虫的日平均飞行次数、平均飞行时间和日飞行规律的差异均不显著(p > 0.05);飞行次数与飞行时间均呈显著正相关(雌蝶:r= 0.978,p < 0.05;雄蝶:r=0.957,p < 0.05)。金斑蝶雌雄成虫羽化次日开始取食,自羽化第2天起,雌雄成虫的日平均取食次数及日平均取食时间均逐渐增加,雄虫的日取食活动高峰期在9:00—11:00,雌虫日访花高峰期在11:00—13:00和15:00—17:00,雌雄成虫的日平均取食次数、平均取食时间和日取食规律的差异均不显著(p > 0.05);取食次数与取食时间均呈不显著正相关(雌蝶:r= 0.949,p > 0.05;雄蝶:r=0.853,p > 0.05)。最早交配时间发生在羽化第4天,雌雄成虫均可多次交配,交配主要发生在14:00—16:00。产卵时间主要在11:00—13:00,雌成虫的产卵方式为散产,主要产卵于寄主植物叶片背面。 结论 金斑蝶成虫期可分为运动器官成熟阶段、补充营养和促进生殖器官发育阶段、求偶和交配阶段、产卵等4个阶段,各阶段内行为有交叉。 Abstract:Objective To study the behavior characteristics of the adultDanaus chrysippus. Method The adult butterflies D. chrysippus were observed by tracking the flying, feeding, courtship, mating and ovipositing behavior in the field of the net-house. Result The eclosion mainly occurred at the 8:00—10:00. The adults were in the stop or rest status at the day of emergence. The daily average flying time and frequencies gradually increased from the second day of eclosion to the day of mating. The flying peak time of males were at 13:00—15:00, while two flying peak were observed in females at 9:00—11:00 and 15:00—17:00. There was no significant difference between male and female adults in the daily average flight number, times and the daily flight rule (p > 0.05). However, there was a significant positive correlation between the number of flights and the time of flight in both sex (p < 0.05). The feeding behavior began at the second day of eclosion. The daily average feeding time and frequencies also gradually increased. The daily feeding activity peak of male is 9:00—11:00, on the female flower visiting peak is 11:00—13:00 and 15:00—17:00. There was no significant difference between male and female adults in the daily average feeding number, times and the daily feeding rule (p > 0.05), and no significant positive correlation was found between the feeding frequency and feeding time in both sex (p > 0.05). The first mating behavior occurred at the fourth day after eclosion. The male and female can mate more than once in their whole lives. Mating occurred mainly at 14:00—16:00, while egg-laying occurred mainly at 11:00—13:00. Most of eggs were deposited in a dispersed manner on the back of host leaves. Conclusion The adult stage of D. chrysippus can be divided into four, i.e. motion organ mature stage, nutritional supplements and promote reproductive organ development stage, courtship and mating stage, and oviposition stage. In each stage, the behavior has a cross. -
Key words:
- flight behavior
- / feeding behavior
- / courtship behavior
- / mating behavior
- / egg-laying behavior
-
表 1 金斑蝶羽化时间
Table 1. The eclosion time of Danaus chrysippus
雄蝶Male 雌蝶Female 编号No. 羽化时间Eclosion time 编号No. 羽化时间Eclosion time 1 6:46:00 4 7:53:19 2 7:25:36 5 7:57:52 3 8:40:01 6 9:48:18 7 9:26:04 10 8:14:34 8 9:30:54 11 8:33:54 9 8:44:20 12 8:51:25 13 9:16:15 16 8:52:13 14 9:09:59 17 9:47:36 15 9:16:15 18 10:36:01 19 9:50:02 20 10:22:40 21 7:36:49 29 8:18:07 22 8:10:10 30 8:21:40 23 8:48:20 31 8:45:54 24 8:58:58 32 8:50:47 25 9:03:02 33 9:05:14 26 9:05:20 34 9:16:53 27 9:09:59 35 9:38:11 28 9:6:15 36 9:40:46 -
[1] 吴少会, 向群, 薛芳森. 昆虫的行为节律[J]. 江西植保, 2006, 29(4): 147-157. doi: 10.3969/j.issn.2095-3704.2006.04.001 [2] 王翻艳, 李承哲, 陈晓鸣, 等. 大帛斑蝶成虫行为学特征[J]. 生态学报, 2015, 35(23): 1-8. [3] Li C Z, Wang F Y, Chen X M, et al. Adult Behavior of Tirumala limniace(Lepidoptera: Danaidae)[J]. Journal of Insect Science, 2015, 15(1): 1-7. doi: 10.1093/jisesa/ieu165 [4] 曾菊平, 周善义, 丁健, 等. 濒危物种金斑喙凤蝶的行为特征及其对生境的适应性[J]. 生态学报, 2012, 32(20): 6527-6534. [5] 周成理. 枯叶蛱蝶生物学特征及种内分化的分子遗传研究[D]. 北京: 中国林业科学研究院, 2008. [6] 包正云. 青海祁连山地区四川绢蝶的访花行为和繁殖生态学研究[D]. 西宁: 青海师范大学, 2010. [7] 王文明. 中华虎凤蝶和金斑蝶在燕山地区的生物学特性研究[D]. 南昌: 南昌大学, 2011. [8] Andersson S, Dobson H E M. Behavioral foraging responses by the butterfly Heliconius melpomene to Lantana camara floral scent[J]. Journal of Chemical Ecology, 2003, 29(10): 2303-2318. doi: 10.1023/A:1026226514968 [9] Honda K, Ômura H, Hayashi N. Identification of floral volatiles from Ligustrum japonicum that stimulate flower-visiting by cabbage butterfly, Pieris rapae[J]. Journal of Chemical Ecology, 1998, 24(12): 2167-2180. doi: 10.1023/A:1020750029362 [10] Lewis Z, Wedell N. Effect of adult feeding on male mating behav-iour in the butterfly, Bicyclus anynana (Lepidoptera: Nymphali-dae). [J]. Journal of Insect Behavior, 2007, 20 (2): 201-213. . doi: 10.1007/s10905-007-9075-2 [11] Ômura H, Honda K. Behavioral and electroantennographic responsiveness of adult butterflies of six nymphalid species to food-derived volatiles[J]. Chemoecology, 2009, 19(4): 227-234. doi: 10.1007/s00049-009-0024-8 [12] Costanzo K, Monteiro A. The use of chemical and visual cues in female choice in the butterfly Bicyclus anynana[J]. Proceedings Biological Sciences, 2007, 274(1611): 845-851. [13] Nishida R, Schulz S, Kim C S, et al. Male sex pheromone of a giant danaine butterfly, Idea leuconoe[J]. Journal of Chemical Ecology, 1996, 22(5): 949-972. doi: 10.1007/BF02029947 [14] Bruinsma M, Van Dam N M, Van Loon J J A, et al. Jasmonic acid-induced changes in Brassica oleracea affect oviposition preference of two specialist herbivores[J]. Journal of chemical ecology, 2007, 33(4): 655-668. doi: 10.1007/s10886-006-9245-2 [15] Stefanescu C, Penuelas J, Sardans J, et al. Females of the specialist butterfly Euphydryas aurinia(Lepidoptera: Nymphalinae: Melitaeini)select the greenest leaves of Lonicera implexa(Caprifoliaceae)for oviposition[J]. European Journal of Entomology, 2006, 103(3): 569-574. doi: 10.14411/eje.2006.077 [16] Catta-Preta P D, Zucoloto F S. Oviposition behavior and performance aspects of Ascia monuste(Godart, 1919)(Lepidoptera, Pieridae)on kale(Brassica oleracea var. acephala)[J]. Revista Brasileira de Entomologia, 2003, 47(2): 169-174. doi: 10.1590/S0085-56262003000200003 [17] 周尧. 中国蝶类志[M]. 郑州: 河南科学技术出版社, 1994. [18] 陈晓鸣, 石雷, 周成理, 等. 中国观赏蝴蝶[M]. 北京: 中国林业出版社, 2008. [19] Tang Y C, Zhou C L, Chen X M, et al. Visual and Olfactory Responses of Seven Butterfly Species During Foraging[J]. Journal of Insect Behavior, 2013, 26(3): 387-401. doi: 10.1007/s10905-012-9358-0 [20] 张军生, 滕文霞, 康尔年. 红线蛱蝶生物学特性初步研究[J]. 内蒙古林业科技, 2002(1): 20-22. doi: 10.3969/j.issn.1007-4066.2002.01.007 [21] 佘德松, 冯福娟. 木兰青凤蝶生物学特性研究[J]. 中国森林病虫, 2003, 22(6): 17-20. doi: 10.3969/j.issn.1671-0886.2003.06.007 [22] 周成理, 史军义, 易传辉, 等. 枯叶蛱蝶Kallima inachus的生物学研究[J]. 四川动物, 2005, 24(4): 445-450. doi: 10.3969/j.issn.1000-7083.2005.04.001 [23] 任志勇, 朱道弘, 王洪建. 花椒凤蝶生物学特性观察及防治试验初报[J]. 甘肃林业科技, 2007, 32(4): 54-56. doi: 10.3969/j.issn.1006-0960.2007.04.015 [24] 廖宇. 玉带凤蝶生物学特性研究[D]. 福州: 福建农林大学, 2009. [25] 袁德成, 买国庆, 薛大勇, 等. 中华虎凤蝶栖息地、生物学和保护现状[J]. 生物多样性, 1998, 6(2): 105-115. doi: 10.3321/j.issn:1005-0094.1998.02.005 [26] 罗志文, 李世震, 李春丰, 等. 丝带凤蝶的生物学特性研究初报[J]. 佳木斯大学学报: 自然科学版, 2005, 23(3): 437-442. doi: 10.3969/j.issn.1008-1402.2005.03.032 [27] Fernanda C F, Carminda C L. Differential flight muscle development in workers, queens and males of the eusocial bees, Apis mellifera and Scaptotrigona postica[J]. Journal of Insect Science, 2010, 10(85): 1-9. doi: 10.1673/031.010.8501 [28] Hirota T, Hamano K, Obara Y. The Influence of Female Post-Emergence Behavior on the Time Schedule of Male Mate-Locating in Pieris rapae crucivora[J]. Zoologicalence, 2001, 18(4): 475-482. [29] 霍晓杰. 青海祁连山地区四川绢蝶的生物学特性及各因素对其活动影响的研究[D]. 西宁: 青海师范大学, 2010. [30] 刘光华, 陆永跃, 甘咏红, 等. 曲纹紫灰蝶的生物学特性和发生动态研究[J]. 应用昆虫学报, 2003, 40(5): 426-428. doi: 10.3969/j.issn.0452-8255.2003.05.010 [31] 王翻艳. 大帛斑蝶成虫行为学观察及其求偶机制研究[D]. 北京: 中国林业科学研究院, 2015. [32] 邵长芬, 关文灵, 李得发, 等. 大叶醉鱼草访花昆虫行为与活动规律[J]. 亚热带植物科学, 2014(3): 227-231. doi: 10.3969/j.issn.1009-7791.2014.03.009 [33] O'Brien D M, Boggs C L, Fogel M L. Making eggs from nectar: connections between butterfly life history and the importance of nectar carbon in reproduction[J]. Oikos, 2004, 105(2): 279-291. doi: 10.1111/j.0030-1299.2004.13012.x [34] Mevi-Schütz J, Erhardt A. Amino acids in nectar enhance butterfly fecundity: a long-awaited link[J]. American Naturalist, 2005, 165(4): 411-419. doi: 10.1086/429150 [35] Baguette M, Schtickzelle N. Local population dynamics are important to the conservation of metapopulations in highly fragmented landscapes[J]. Journal of Applied Ecology, 2003, 40(2): 404-412. doi: 10.1046/j.1365-2664.2003.00791.x -





 下载:
下载: