-
近年来,随着植物次生代谢研究手段的提高及有色光源条件的发展,光照对植物次生代谢的影响及其机理研究引起国内外学者的广泛关注[1-3]。许多研究表明,光质的不同不仅影响植物的初生代谢和生长状态,而且还会影响植物的次生代谢过程[4-5]。如黄膜促进了2年生毛脉酸模(Rumex gmelinii Turcz. ex Ledeb)中蒽醌类成分的合成[6];橙光和红光有利于耐荫药用植物绞股蓝(Gynostemma pentaphyllum (Thunb.) Makino)的生长和总皂甙积累[7];蓝膜处理后白桦(Betula platyphylla Sukaczev)愈伤组织中三萜累积量增加[8]。在实验室条件下可通过不同颜色的滤光片和荧光灯来获得不同光质,在大田生产中可通过不同颜色的滤光膜来实现不同的光质处理。利用不同颜色的滤光膜研究其生长状况及次生代谢产物的变化,不仅可以为道地药材形成的机理和次生代谢途径分析提供理论依据,而且在生产实践中提高次生代谢产物的产率具有重要意义。
三叶崖爬藤(Tetrastigma hemsleyanum Diels et Gilg)为葡萄科(Vitaceae)崖爬藤属(Albertisia Becc.)植物,又名三叶青、蛇附子、石老鼠、石猴子,为中国特有珍稀药用植物,广泛分布于长江以南各省份,常生于山坡林下的灌丛中或山谷溪边林下的岩石缝中,生长海拔300~1 300 m。全株供药用,有活血散瘀、解毒、化痰的作用,临床用于治疗病毒性脑膜炎、乙型脑炎、病毒性肺炎、黄胆性肝炎等,其块茎对小儿高烧有特效。三叶崖爬藤虽然分布广泛,但多年来对野生资源的过度利用,再加上对分布区自然环境的破坏,已经导致其野生群体数量锐减。近年来,对三叶崖爬藤的研究主要集中在药用价值[9-10]、组织培养[11-12]和化学成分[13-14]等方面。三叶崖爬藤人工栽培的研究起步较晚,目前三叶崖爬藤野生驯化栽培中,仅对光、肥、水因子进行了初步研究,大田生产中三叶崖爬藤遮光的研究也有报道[15],但有关光质对三叶崖爬藤的影响研究还未见报道。本试验以浙江绍兴紫藤三叶崖爬藤为研究材料,通过研究不同光质条件下三叶崖爬藤的生物量及有效成分的积累,旨在筛选能有效提高三叶崖爬藤产量的光质条件,为三叶崖爬藤规范化种植提供理论依据和技术支持。
-
试验地位于浙江绍兴市平水镇会稽山基地,地处中纬度亚热带北缘的过渡地带(120 ° 46 ′39 ″ E,29 °42 ′02 ″ N)。该试验地属东西季风湿润气候区,全年温暖湿润,冷暖空气交替影响,冬冷夏热,四季分明,冬夏长,春秋短,年平均气温16.9℃。光照较充足,小气候资源丰富,年平均日照时数约1 782 h,7、8月日照时数最多,2月日照时数最少。雨量充沛,年平均降水量为1 403.0 mm。土壤类型多为红壤,具有黏、酸、瘦等主要肥力特征,旱季保水性能差。
三叶崖爬藤采用盆栽育苗,既方便水肥管理,也便于后期块茎的采收。以无性繁殖及来源相同、长势一致的2年生三叶崖爬藤扦插盆栽苗为材料。
-
试验以太阳光透光率相近的特制不同颜色的滤光膜得到的不同光质,单因素5水平随机区组设计,重复3次。所用光膜购于上海伟康有色塑料厂,分别为红色光膜(波长620~780 nm,波峰662 nm,标记为R)、黄色光膜(波长560~590 nm,波峰570 nm,标记为Y)、绿色光膜(波长460~500 nm,波峰480 nm,标记为G)、蓝色光膜(波长400~450 nm,波峰420 nm,标记为B)和白色光膜(标记为W),透光率均为85%。试验以白色光膜为对照处理。于2016年4月初用竹竿搭建遮阴棚进行光质处理,搭建高度约110 cm,顶部及四周均用滤光膜盖住,下部距地面30 cm,以利通风,防止遮光棚温度过高。
-
于2017年11月中旬,随机选取三叶崖爬藤植株成熟的叶片,样品采集完后装入冰盒带回,用MRS-9600TFU2L叶面积仪(上海中晶科技有限公司生产)测定新鲜叶片叶长、叶宽、叶面积等指标,分析不同光质对叶形态指标的影响。
-
于2017年11月中旬,随机选取三叶崖爬藤植株成熟的叶片,样品采集完后装入冰盒带回,在实验室经自来水冲洗、蒸馏水清洗,去中脉,剪碎至小于1 mm的细丝,混匀,准确称取0.05 g,用浸提法测定叶绿素含量;清洗后的叶片用液氮研磨,准确称取0.20 g,用考马斯亮蓝G-250法测定可溶性蛋白含量;烘干处理后的叶片去中脉,磨碎,混匀,准确称取0.20 g,采用蒽酮法测定可溶性糖含量。每个处理测定3次,每次选取3~5片叶片。
-
于2017年11月中旬,将三叶崖爬藤整株挖起洗净,擦干表面水分后用万分之一电子天平称量每盆的地上部分、地下部分鲜质量,每个处理测量15盆,称量鲜质量后放置烘箱105℃杀青0.5 h,然后置于80℃烘干至恒质量,再分别称其地上部分、地下部分干质量。
-
(1) 对照品溶液的制备:精密称取在120℃干燥至恒质量的芦丁对照品50 mg(中国食品药品检定研究院,100080-201610),置25 mL量瓶中,加甲醇适量,置水浴上微热使溶解,放冷,加甲醇至刻度,摇匀。精密量取10 mL,置100 mL量瓶中,加水至刻度,摇匀,即得(每l mL中含芦丁0.2 mg)。(2)标准曲线的制备:精密量取对照品溶液1、2、3、4、5、6 mL, 分别置25 mL量瓶中,各加水至6 mL, 加5%亚硝酸钠溶液1 mL,摇匀, 放置6 min,加10%硝酸铝溶液1 mL,摇匀,放置6 min, 加氢氧化钠试液10 mL, 再加水至刻度,摇匀,放置15 min,以相应试剂为空白,立即照紫外-可见分光光度法, 在500 nm的波长处测定吸光度,以吸光度为纵坐标,浓度为横坐标,绘制标准曲线。(3)样品溶液制备:取本品细粉约4 g,用甲醇回流提取2次(分别为50 mL甲醇,时间为1 h),滤液浓缩至干,用10 mL甲醇溶解至100 mL容量瓶中,用水定容至100 mL,摇匀。取3 mL,置25 mL量瓶中,照标准曲线制备项下的方法,自“加水至6 mL”起按相同步骤测定吸光度,从标准曲线上读出供试品溶液中芦丁的质量,计算,即得总黄酮含量。(4)空白溶液制备:取10%甲醇3 mL,置25 mL量瓶中,照标准曲线制备项下的方法,自“加水至6 mL”起按相同步骤操作,即得空白溶液。
-
使用Exce l 2007以及SPSS 13.0统计软件进行数据分析和制图。
-
从不同光质处理下三叶崖爬藤叶片叶形参数测定结果(表 1)可以看出:不同的光质对三叶崖爬藤叶长、叶宽及叶面积有较大的影响,对叶宽/叶长及变异系数影响不明显。红光、黄光、绿光处理下的三叶青叶长、叶宽和叶面积均高于白光处理,蓝光处理下的三叶崖爬藤叶长、叶宽和叶面积均低于白光处理,且绿光处理下的三叶崖爬藤叶片叶形指标均最大,蓝光处理下的三叶崖爬藤叶长、叶宽和叶面积均最小。因此,在绿光、红光和黄光处理下三叶崖爬藤叶长、叶宽及叶面积均较大,而蓝光处理不利于三叶崖爬藤叶片的生长。
表 1 不同光质处理下三叶崖爬藤叶片叶形参数
Table 1. Morphological parameters of leaves in T. hemsleyanum under different light quality treatments
处理Treatment 叶长Length/cm 叶宽Width/cm 叶面积Area/cm2 叶宽/叶长Width/Length 变异系数Form coefficient W(CK) 4.53±0.61c 1.98±0.20c 5.87±1.04c 0.44±0.07b 0.57±0.07b R 5.13±0.66b 2.29±0.30b 7.63±1.72b 0.45±0.05b 0.58±0.07b Y 5.08±0.64b 2.26±0.30b 7.39±1.67b 0.45±0.06b 0.56±0.08b G 6.52±0.97a 3.18±0.45a 13.90±3.97a 0.49±0.06a 0.64±0.07a B 4.36±0.50c 1.96±0.20c 5.61±0.97c 0.45±0.04b 0.58±0.05b 注:同列不同小写字母表示差异显著(P < 0.05),下同。
Note:Date with different lowercase letters in the same column are highly significantly different (P < 0.05), the same below. -
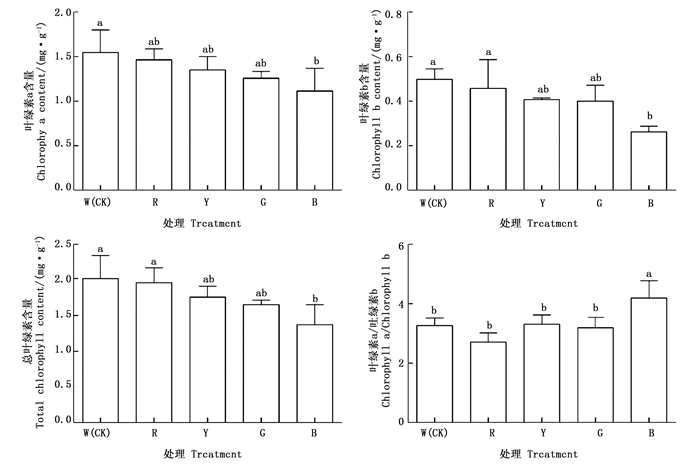
不同光质处理下三叶崖爬藤叶片中光合色素含量的变化见图 1。所有处理中,白光处理叶绿素a含量、叶绿素b含量和总叶绿素含量最高,蓝光处理光合色素含量最低,叶绿素a含量、叶绿素b含量和总叶绿素含量大小排序是白光处理>红光处理>黄光处理>绿光处理>蓝光处理;叶绿素a/b值蓝光处理最高,红光处理最低,叶绿素a/叶绿素b大小排序是蓝光处理>黄光处理>白光处理>绿光处理>红光处理。可见白光处理下三叶崖爬藤叶片中光合色素含量最高,蓝光处理则不利于三叶崖爬藤叶片中光合色素含量的积累。
-
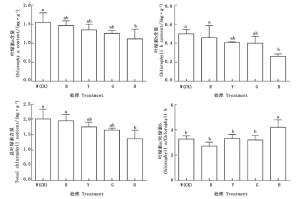
不同光质处理下三叶崖爬藤叶片可溶性蛋白和可溶性糖含量的变化见图 2。三叶崖爬藤叶片中可溶性蛋白含量蓝光处理最高,红光处理最低,蓝光处理与白光处理差异显著,其它各组处理与白光处理均差异不显著。说明蓝光处理能提高三叶崖爬藤叶片中可溶性蛋白的含量,而红光处理降低其含量。可溶性糖含量红光处理最高,蓝光处理最低,红光处理与黄光处理差异不显著,但各处理与白光处理间均差异显著。可以看出,红光处理提高了三叶崖爬藤叶片中可溶性糖含量,而在蓝光处理下其含量最低。
-
不同光质处理下三叶崖爬藤地上部分、地下部分生物量测定结果见表 2。三叶崖爬藤地上鲜质量、地上干质量、总鲜质量和总干质量大小排序为红光处理>白光处理>绿光处理>黄光处理>蓝光处理,地下鲜质量和地下干质量大小排序为红光处理>绿光处理>白光处理>黄光处理>蓝光处理,红光处理下三叶崖爬藤地上部分、地下部分生物量最大,蓝光处理下其地上部分、地下部分生物量最小,说明红光处理有利于三叶崖爬藤生物量的积累,而蓝光处理则不利于其生物量的积累。
表 2 不同光质处理下三叶崖爬藤总生物量及分配
Table 2. Effects of different light quality treatments on total biomass and distribution in T. hemsleyanum
处理
Treatment地上鲜质量
Fresh weight overground/g地下鲜质量
Fresh weight underground/g总鲜质量
Total fresh weight/g地上干质量
Dry weight overground/g地下干质量
Dry weight underground/g总干质量/g
Total dry weight/gW(CK) 148.44±16.96ab 107.34±41.63a 255.78±29.31a 49.06±8.03a 43.76±13.77a 95.96±32.73a R 186.64±43.61a 115.19±34.73a 301.83±60.15a 49.15±9.34a 46.90±25.28a 92.91±17.26ab Y 81.87±15.38c 72.67±17.84a 154.54±33.07b 25.83±4.39bc 26.11±5.21a 51.94±9.53bcd G 126.29±33.88b 112.33±46.66a 238.62±44.13a 41.55±15.63ab 43.96±22.22a 85.51±17.70abc B 58.60±9.86c 67.14±16.66a 125.74±26.08b 25.63±3.72bc 23.67±8.61a 49.30±5.76bd -
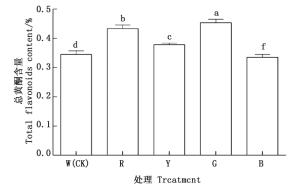
由图 3可以看出:不同光质处理下三叶崖爬藤块茎中总黄酮含量存在差异性。绿光处理下总黄酮含量最高,其含量为0.456%,其次是红光处理,总黄酮含量为0.431%,总黄酮含量最低的为蓝光处理,为0.338%,最高含量是最低含量的1.35倍。说明红光和绿光处理能促进三叶崖爬藤块茎中总黄酮含量的积累,蓝光处理则不利于总黄酮含量的积累。
-
光质能影响叶片中叶绿素含量,红光可提高草莓(Fragaria ananassa (Weston) Duchesne)、一品红(Euphorbia pulcherrima Willd. ex Klotzsch)等植物叶片中叶绿素a、叶绿素b以及总叶绿素含量[16-17];蓝光可显著提高莴苣(Lactuca sativa L.)和番茄(Lycopersicon esculentum Mill.)幼苗叶片叶绿素a和类胡萝卜素含量[18],促进风信子(Hyacinthus orientals L.)愈伤组织叶绿素的形成[19]。本试验结果表明,红光处理能提高叶绿素a、叶绿素b和总叶绿素含量,蓝光处理叶绿素a、叶绿素b和总叶绿素含量最低。表明不同光质对叶绿素含量的影响并不一致,这可能是由于物种差异,光质对植物细胞色素含量的影响也会有所不同。
光质对植物的氮代谢有重要的调节作用,有研究发现,蓝光可提高植株内可溶性蛋白含量[20-21]。本试验结果表明,蓝光处理能提高三叶崖爬藤叶片中可溶性蛋白的含量,而红光处理降低了其含量,这说明蓝光能促进新合成的有机物中蛋白质的积累,提高蛋白质含量,这与Kowallik[22]、陈强等[23]研究结果一致。蓝光对NR有激活作用[24],从而为蛋白质的合成提供了较多的可同化态的氮源。蛋白质是大分子物质,合成需要更多能量,而蓝光区光量子能量较高,因此,蓝光促进蛋白质的合成也可能与光质能量有关。
光质对植物可溶性糖的含量有重要影响,在红光下生长的植物碳水化合物含量较高[25-26]。本试验结果表明,红光处理能提高三叶崖爬藤叶片中可溶性糖含量,而蓝光处理降低了可溶性糖含量,这与蒲高斌等[27]、陈强等[23]的研究结果一致。原因可能是红光处理下三叶崖爬藤光合色素含量较高,光合作用产物较多,而蓝光处理下三叶崖爬藤光合色素含量最低,故其可溶性糖含量较低;也可能是蓝光处理下三叶崖爬藤的呼吸速率较高,光合作用产物消耗较多。
红光可促进幼苗的生长,红光处理的幼苗干物质积累多,营养生长旺盛。在番茄、茄子(Solanum melongena L.)及黄瓜(Cucumis sativus L.)等作物中也有类似的发现[28-29]。本试验结果表明,在红光处理下三叶崖爬藤地上部分和地下部分的生物量均最大,与以上研究类似。
光是植物生命活动的重要环境因子之一,它不仅是植物生长发育的能量来源,而且作为信号因子调控植物的生长发育。本试验中,除蓝光处理外,不同滤光膜下生长的三叶崖爬藤块茎中总黄酮含量都高于白光处理,而且在绿光处理和红光处理下最显著。这说明滤光膜造成的光质环境有利于总黄酮在三叶崖爬藤块茎中积累,绿膜和红膜的这种促进作用尤为明显。已有的结果表明[30-31],当研究部位为叶时,短波段光如蓝光促进黄酮类化合物的积累,长波段光如红光抑制其积累。而关于光质对植物根中黄酮类化合物的影响研究较少。光质对叶和根中黄酮类化合物的积累变化规律是否一致,还有待于进一步研究发现。
-
本试验结果表明,光质对三叶崖爬藤的生长及有效成分含量均有影响,在红光处理下,三叶崖爬藤的叶长、叶宽及叶面积均较佳,光合色素含量较高,作为光合作用产物之一的可溶性糖含量也最高,其地上部分和地下部分生物量最大,并且三叶崖爬藤块茎中总黄酮含量较佳,所以在三叶崖爬藤的人工栽培中可以利用红光来提高其产量及有效成分含量。
不同光质对三叶崖爬藤生长及有效成分含量的影响
Effects of Light Quality on the Growth and Content of Active Ingredients of Tetrastigma hemsleyanum
-
摘要:
目的 研究不同光质处理下三叶崖爬藤生长及有效成分含量变化,以确定适宜三叶崖爬藤生长的最适光质条件。 方法 以2年生三叶崖爬藤为材料,用不同颜色的滤光膜(红色、黄色、绿色、蓝色和白色)进行光质处理,测定三叶崖爬藤叶片的叶形指标、生理指标、生物量及块茎中总黄酮含量。 结果 表明:红光处理下的三叶崖爬藤在叶形指标、生理指标、生物量和总黄酮含量上均得到改善,而其余光质处理结果仅对其中某一指标有所改善。 结论 红光处理下的三叶崖爬藤块茎的产量和质量均较佳,在三叶崖爬藤人工栽培中可以利用红光提高其产量及有效成分含量。 Abstract:Objective The growth and content of active constituents of Tetrastigma hemsleyanum under different light quality treatments were studied to determine the optimum light quality conditions for the growth of T. hemsleyanum. Method Two-year-old T. hemsleyanum was used as the material, and the light quality treatment was carried out with different color filter membranes (red, yellow, green, blue, and white light). The leaf shape index, physiological index, biomass and total flavonoid content in the tuber of T. hemsleyanum were determined. Result The result suggests that the red light treatments do have impact on the growth and active ingredients of T. hemsleyanum. Red light treatment promotes both the growth and active ingredients of T. hemsleyanum while the other treatments promote just one aspect of them. Conclusion The yield and quality of T. hemsleyanum under red light treatment are better. Red light can be used to increase the yield and active ingredient content in the artificial cultivation of T. hemsleyanum. -
Key words:
- Tetrastigma hemsleyanum
- / light quality
- / physiology
- / biomass
- / active ingredients
-
表 1 不同光质处理下三叶崖爬藤叶片叶形参数
Table 1. Morphological parameters of leaves in T. hemsleyanum under different light quality treatments
处理Treatment 叶长Length/cm 叶宽Width/cm 叶面积Area/cm2 叶宽/叶长Width/Length 变异系数Form coefficient W(CK) 4.53±0.61c 1.98±0.20c 5.87±1.04c 0.44±0.07b 0.57±0.07b R 5.13±0.66b 2.29±0.30b 7.63±1.72b 0.45±0.05b 0.58±0.07b Y 5.08±0.64b 2.26±0.30b 7.39±1.67b 0.45±0.06b 0.56±0.08b G 6.52±0.97a 3.18±0.45a 13.90±3.97a 0.49±0.06a 0.64±0.07a B 4.36±0.50c 1.96±0.20c 5.61±0.97c 0.45±0.04b 0.58±0.05b 注:同列不同小写字母表示差异显著(P < 0.05),下同。
Note:Date with different lowercase letters in the same column are highly significantly different (P < 0.05), the same below.表 2 不同光质处理下三叶崖爬藤总生物量及分配
Table 2. Effects of different light quality treatments on total biomass and distribution in T. hemsleyanum
处理
Treatment地上鲜质量
Fresh weight overground/g地下鲜质量
Fresh weight underground/g总鲜质量
Total fresh weight/g地上干质量
Dry weight overground/g地下干质量
Dry weight underground/g总干质量/g
Total dry weight/gW(CK) 148.44±16.96ab 107.34±41.63a 255.78±29.31a 49.06±8.03a 43.76±13.77a 95.96±32.73a R 186.64±43.61a 115.19±34.73a 301.83±60.15a 49.15±9.34a 46.90±25.28a 92.91±17.26ab Y 81.87±15.38c 72.67±17.84a 154.54±33.07b 25.83±4.39bc 26.11±5.21a 51.94±9.53bcd G 126.29±33.88b 112.33±46.66a 238.62±44.13a 41.55±15.63ab 43.96±22.22a 85.51±17.70abc B 58.60±9.86c 67.14±16.66a 125.74±26.08b 25.63±3.72bc 23.67±8.61a 49.30±5.76bd -
[1] Folta K M, Maruhnich S A.Green light:a signal to slow down or stop[J].Journal of Experimental Botany, 2007, 58(12):3099-3111. doi: 10.1093/jxb/erm130 [2] Pérez-Balibrea S, Moreno D A, García-Viguera C.Influence of light on health-promoting phytochemicals of broccoli sprouts[J].Journal of the Science of Food & Agriculture, 2010, 88(5):904-910. [3] Schreiner M, Krumbein A, Mewis I, et al.Short-term and moderate UV-B radiation effects on secondary plant metabolism in different organs of nasturtium (Tropaeolum majus L.)[J].Innovative Food Science & Emerging Technologies, 2009, 10(1):93-96. [4] 阎秀峰, 王洋, 尚辛亥.温室栽培光强和光质对高山红景天生物量和红景天甙含量的影响[J].生态学报, 2003, 23(5):841-849. doi: 10.3321/j.issn:1000-0933.2003.05.001 [5] 阎秀峰, 王洋, 郭盛磊, 等.遮荫和红膜处理对高山红景天根生物量及红景天甙含量季节变化的影响[J].应用生态学报, 2004, 15(3):382-386. doi: 10.3321/j.issn:1001-9332.2004.03.006 [6] 马伟, 王振月, 陈立超, 等.不同光质对毛脉酸模中蒽醌类成分的影响[J].植物研究, 2007, 27(6):763-769. doi: 10.3969/j.issn.1673-5102.2007.06.021 [7] 刘世彪, 李馨芸, 李朝阳, 等.影响绞股蓝和五柱绞股蓝生长和总皂甙积累的有效光质研究[J].热带作物学报, 2011, 32(1):50-54. doi: 10.3969/j.issn.1000-2561.2011.01.010 [8] 范桂枝, 詹亚光, 王博, 等.光质、光周期对白桦愈伤组织生长和三萜质量分数的影响[J].东北林业大学学报, 2009, 37(1):1-3. doi: 10.3969/j.issn.1000-5382.2009.01.001 [9] 李华美, 浦锦宝, 郑军献, 等.三叶青乙酸乙酯提取物对小鼠Lewis肺癌移植性肿瘤的抑制作用及免疫功能的影响[J].中国中医药科技, 2012, 19(3):229-230. doi: 10.3969/j.issn.1005-7072.2012.03.024 [10] 钟良瑞, 魏克民.三叶青黄酮对肺癌A549细胞生长抑制与MAPKs通路关系的研究[J].中国药理学通报, 2014, 30(1):101-104. doi: 10.3969/j.issn.1001-1978.2014.01.022 [11] 彭昕, 林言娜, 何军邀.正交法优化三叶青继代增殖与生根培养的条件[J].现代中药研究与实践, 2012, 26(2):10-12. [12] 王静, 郭万里, 孔亚泽, 等.珍稀药用植物三叶青的高效微繁体系研究[J].浙江理工大学学报, 2016, 35(4):636-642. [13] 霍昕, 杨迺嘉, 刘文炜, 等.三叶青块根乙醚提取物成分研究[J].药物分析杂志, 2008, 28(10):1651-1653. [14] 许文, 傅志勤, 林婧, 等.UPLC-MS/MS法同时测定三叶青中10种黄酮类成分[J].药学学报, 2014, 49(12):1711-1717. [15] Dai Y, Shen Z G, Ying L, et al.Effects of shade treatments on the photosynthetic capacity, chlorophyll fluorescence, and chlorophyll content of Tetrastigma hemsleyanum Diels et Gilg[J].Environmental & Experimental Botany, 2009, 65(3):177-182. [16] 徐凯, 郭延平, 张上隆.不同光质对草莓叶片光合作用和叶绿素荧光的影响[J].中国农业科学, 2005, 38(2):369-375. doi: 10.3321/j.issn:0578-1752.2005.02.024 [17] 江明艳, 潘远智.不同光质对盆栽一品红光合特性及生长的影响[J].园艺学报, 2006, 33(2):338-343. doi: 10.3321/j.issn:0513-353X.2006.02.022 [18] 张欢, 徐志刚, 崔瑾, 等.光质对番茄和莴苣幼苗生长及叶绿体超微结构的影响[J].应用生态学报, 2010, 21(4):959-965. [19] Anna B, Anna K.Effect of light quality on somatic embryogenesis in Hyacinthus orientals L.'Delft's Blue'[J].Biological Bulletin of Poznan, 2001, 38(1):103-107. [20] 杨晓建, 刘世琦, 张自坤, 等.不同发光二极管对青蒜苗营养品质的影响[J].营养学报, 2010, 32(5):518-520. [21] 邢泽南, 张丹, 李薇, 等.光质对油葵芽苗菜生长和品质的影响[J].南京农业大学学报, 2012, 35(3):47-51. [22] Kowallik W.Blue light effects on respiration[J].Plant Biology, 1982, 33(33):51-72. [23] 陈强, 刘世琦, 张自坤, 等.不同LED光源对番茄果实转色期品质的影响[J].农业工程学报, 2009, 25(5):156-161. doi: 10.3969/j.issn.1002-6819.2009.05.30 [24] Campbell W H.Nitrate reductase biochemistry comes of age[J].Plant Physiology, 1996, 111(2):355-361. doi: 10.1104/pp.111.2.355 [25] Shao-Shan L I, Pan R C.Effect of blue light on the metabolism of carbohydrate and protein in rice (Oryza Sativa L.) seedlings[J].Acta Phytophisiologica Sinica, 1995, 21(1):22-28. [26] Shin K S, Murthy H N, Heo J W, et al.Induction of betalain pigmentation in hairy roots of red beet under different radiation sources[J].Biologia Plantarum, 2003, 47(1):149-152. [27] 蒲高斌, 刘世琦, 刘磊, 等.不同光质对番茄幼苗生长和生理特性的影响[J].园艺学报, 2005, 32(3):420-425. doi: 10.3321/j.issn:0513-353X.2005.03.008 [28] 马光恕, 廉华, 闫明伟.不同覆盖材料对大棚内番茄生长发育的影响[J].东北农业科学, 2002, 27(4):41-43. [29] 傅明华, 汪羞德.多功能转光塑料薄膜应用效应研究[J].农业工程学报, 2000, 16(6):81-84. [30] Thwe A A, Kim Y B, Li X, et al.Effects of light-emitting diodes on expression of phenylpropanoid biosynthetic genes and accumulation of phenylpropanoids in Fagopyrum tataricum sprouts[J].Journal of Agricultural & Food Chemistry, 2014, 62(21):4839-4845. [31] Ouzounis T, Parjikolaei B R, Fretté X, et al.Predawn and high intensity application of supplemental blue light decreases the quantum yield of PSⅡ and enhances the amount of phenolic acids, flavonoids, and pigments in Lactuca sativa[J].Frontiers in Plant Science, 2015, 6:19.doi:10.3389/fpls.015.00019. -




 下载:
下载: