-
银杏(Ginkgo biloba L.)是我国特有的古老而珍贵的孑遗树种,其古树资源丰富,集食用、材用、药用、绿化、生态与观赏于一体,素有“活化石”之称[1]。然而,由于环境和人为影响,高龄银杏古树正面临衰弱和濒危死亡的威胁,因此,保护这些古树已十分迫切。扦插繁殖技术被认为是完整保存古树资源的有效手段之一[2],但不定根的形成受古树树龄、插穗位置、生长调节剂和扦插时间等因素制约[3-4]。此外,高龄古树扦插生根一个亟待解决的问题是插穗采集。因为古树资源珍稀且受法律保护,扦插过程中枝条采集受到明显的限制。所以,尽管已有大量关于扦插生根的研究报道,但仍有必要对银杏枝条不同年龄阶段、部位的扦插生根进行研究,从而探究不同枝条扦插的生根能力,为古树扦插繁育过程中选取更多的插穗提供参考。
枝条部位的选取对于扦插繁殖有明显的差异,如榉树(Zelkova serrata (Thunb.) Makino)、青海云杉(Picea crassifolia Kom.)、油橄榄(Olea europaea L.)、马尾松(Pinus massoniana Lamb.)树冠下部枝条的扦插生根效果明显优于上部枝条,这可能与下部枝条积累了较多的营养物质,为不定根的形成提供更充足的养分有关[5-8]。不定根形成过程中碳水化合物不仅能为根生长提供能量,同时也对防御具有重要的调节作用,如愈伤组织的形成[9-10]。此外,生长相关的初级代谢与防御相关的次级代谢都与碳水化合物含量密切相关[11]。插穗中非结构碳水化合物(NSC),特别是可溶性糖、淀粉与愈伤组织形成密切相关,进而影响不定根的形成。此外,年龄和成熟度对树木形态和生理特性有显著影响,如树高、光合等[12-13],这也影响着不定根生成的能力。如黄栀子(Gardenia jasminoides Ellis)不同枝龄的插穗在不同苗床覆盖物情况下生根差异显著[14];霸王硬枝扦插过程中也发现插穗的龄级是影响扦插的重要因素,其中,1~2年生插穗扦插效果最好[15]。同样,激素对不定根的形成也起着关键的调控作用,如外源IBA可以通过转化为内源的IAA调控不定根相关基因PIN1表达,从而促进不定根的形成[16]。然而,目前还未见有关银杏不同部位、枝龄以及激素处理对扦插生根影响的报道。本研究以50年生银杏南面树冠上、下部1、2、3年生枝条为材料,在全光照喷雾条件下研究不同部位和不同枝龄插穗对不定根形成的影响,并分析了相应位置处叶和茎段中NSC含量变化与其扦插生根的关系,为今后银杏扦插生根机制研究及古树扦插取材提供参考。
-
银杏插穗取自中国林业科学研究院内约50年生的银杏树;基质为中国林业科学研究院生产的无纺布网袋育苗容器轻基质(珍珠岩V:草炭土V=3:1);激素IBA购自Sigma-Aldrich;高效液相色谱仪(HPLC)属于中国林业科学研究院森林生态环境与保护研究所国家林业局森林生态环境重点实验室。
-
2016年7月10日,分别从3棵银杏树南面树冠上部和下部取1年生、2年生、3年生枝段,按单株截取插穗(单株作为1个重复,共3个重复),用于扦插和生理分析;对上述插穗分别进行激素(IBA)和纯水(CK:对照)处理,每个重复至少30根(除下部1年生的至少23根外);扦插前,取上述不同处理插穗上的叶和茎段,测定NSC含量。
-
在中国林科院内,设置高出地面0.5 m,半径6 m的露天圆形插床,插床上方设有可旋转的间歇式自动喷雾装置,前疏后密,两边各置喷头25个。将无纺布轻基质段(10 cm)整齐置于塑料托盘中,扦插前一天用3‰高锰酸钾溶液进行全面消毒,扦插当天用清水浇透,置于插床上备用。
-
选取上述按单株重复采集的健康枝条,根据每年的生长点截取1、2、3年生位置的茎段,制成插穗,长度约6~10 cm,每个插穗保留上部叶1~2片[17]。插穗分别用500 mg·L-1IBA和纯水(CK)处理60 s后进行扦插。
-
扦插前,按照上述单株重复切取未处理插穗基部约2 cm茎段和茎段上部叶片(即单株重复,共3个重复),烘干研磨成粉末,采用HPLC法测定可溶性糖和淀粉含量[18-19]。
糖的提取:称取粉碎好的植物样品0.5~1.0 g,加水50 mL,高压蒸煮2 h,放凉后定容过滤,滤液上机。
淀粉的提取:称取粉碎好的植物样品0.1~0.2 g,用乙醚洗涤4~5次,每次10 mL, 然后用10%乙醇溶液150 mL分次洗涤,弃去滤液,加入蒸馏水10 mL,2:1盐酸1 mL,置沸水水域中回流2.5 h,冷却后用20%氢氧化钠中和,加入13%铝浆[Al2(SO4)·18H2O] 0.5 mL定容过滤,滤液上机。
-
采用旋转式自动喷雾装置,从7:30—18:30开启装置进行间歇式浇水。晴天设置为7:30—9:30和15:30—18:30,每10 min喷雾25 s;9:30—15:30,每5 min喷雾25 s;阴天则每隔2 h喷水25 s,雨天不喷水;每周喷1次500倍多菌灵灭菌,直到试验结束。
-
扦插后每隔1周分别观察上部1年生3个重复的插穗叶片和基部变化状况并拍照。3个月后统计各处理组合的生根率(反正弦值,形成的愈伤也统计在生根率范畴)、生根部位等相关生根指标,实验数据均采用EXCEL和SPSS软件进行统计分析。
-
通过对上部1年生银杏扦插过程中2、4、5、6、8周观察发现:扦插2周时切口处未见明显变化,但4周时切口处开始出现白色愈伤,5周时已出现膨大的愈伤疙瘩,6周时不定根已开始形成,8周时不定根伸长。因此,将银杏扦插过程中不定根形成分为4个阶段,即愈伤形成期(0~4周)、愈伤膨大期(4~6周)、不定根开始形成期(6~8周)、不定根伸长(8周后)。扦插3个月后对生根情况进行统计(表 1)发现:切口处生根占绝大多数,表明银杏主要是愈伤组织生根型。另外,发现部分插穗只有愈伤组织,但未生根。

图 1 银杏上部1年生枝扦插生根过程观察
Figure 1. Observation on rooting process of one-year-old branch in the upper crown of Ginkgo biloba
表 1 银杏扦插不同生根类型的生根率
Table 1. Rooting rates of cutting rooting types in Ginkgo biloba
% 生根类型
Category树冠下部 Lower part of the crown 树冠下部 Lower part of the crown 1年生
Annual2年生
Biennial3年生
Triennial1年生
Annual2年生
Biennial3年生
Triennial切口生根 Rooting at the incision 55 45 42 47 39 30 皮部生根 Rooting at the skin 0 26 0 9 19 0 混合生根 Rooting at the skin and incision 18 9 31 5 10 22 愈伤未生根 Callus 27 21 27 38 31 48 注:各类型百分比指占总生根数量的百分比(%)。 -
枝条年龄是影响不定根形成的重要因素,从图 2可明显看出:树冠上部和下部对照的生根率随枝条年龄的递增而逐渐递减(图中不同大写字母表示P < 0.01显著水平),1~3年生枝条的插穗在树冠上部生根率分别是89.2%、32.7%和22.3%,而下部的生根率分别是81.1%、39.3%和19.8%,枝龄间生根率差异明显,而且1年生远大于2、3年生枝条(P < 0.01)。对照组树冠上部和下部在同枝龄间的生根率没有差异;但IBA处理后,只有3年生枝条上下部的生根率差异极显著(P < 0.01)。结果表明,采集银杏树冠相同方向的上部和下部枝条作为插穗对扦插生根没有明显影响,但枝龄的影响非常明显。
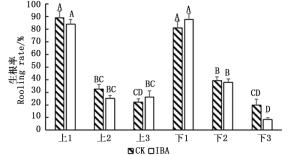
图 2 树冠上部和下部不同枝龄插穗生根情况
Figure 2. Rooting of different-age twigs from the upper and lower crown branches
此外,从图 2还看出:与对照相比,500 mg·L-1IBA处理的上部1、2年生枝条的生根率受到不同程度抑制,分别比对照下降了5.2%和7.6%,但差异不显著(P>0.05),而3年生枝条的生根率比对照提高了3.9%,差异也不显著(P>0.05);IBA处理的下部1、2年生枝条的生根率与对照相比差异均不显著(P>0.05),但3年生枝条的生根率受到了明显抑制,生根率下降了17.82%(P < 0.05)。结果表明,不同部位和枝龄对生长素的响应各异,还需对激素浓度进行优化。
-
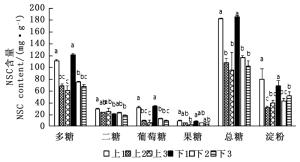
从图 3可看出:树冠下部叶片的总糖、多糖含量明显比树冠上部的高,分别高16%~20%和15%~21%(P < 0.05);葡萄糖和果糖含量也是下部的比上部的高,但差异不显著;二糖含量在上、下部叶片中几乎为零。树冠上部叶片中的淀粉含量是1年生最高,2年生最低,且差异显著(P < 0.05);下部叶片中的淀粉含量3年生的明显大于1、2年生的(P < 0.05)。这表明,树冠上、下部叶片中的糖类和淀粉含量存在明显差异。
从图 4可看出:枝条中的总糖、葡萄糖、多糖含量在树冠上部和下部都是1年生>2年生>3年生,且1年生的远远大于2、3年生的(P < 0.01);果糖和二糖含量未见明显差异(P>0.05);枝条中的淀粉含量在树冠上部和下部的变化也是1年生的远远大于2、3年生的(P < 0.05)。这表明,不同枝龄茎段中总糖、葡萄糖、多糖和淀粉含量存在明显差异。
-
银杏古树资源丰富,不仅是林业重要的活的遗传基因保存库,还是民族历史文化和地域文化“活的见证”,更是大自然和祖先留下来的宝贵财富;然而,却面临着衰弱和濒危死亡的威胁。扦插作为古树无性繁殖的重要手段之一,能完整的保存古树的遗传信息[2, 20-21],但古树受到法律保护,采集枝条时受到严格限制,仅选择1年生枝条作为插穗,远远不能满足扦插的需要,因此,有必要对银杏枝条不同部位及其年龄阶段的扦插生根进行研究,为古树扦插繁育提供借鉴。通过对扦插生根过程的初步观察,本研究将其分为愈伤组织形成期、愈伤组织膨大期、不定根形成期、不定根伸长期4个阶段,并且进一步证明了银杏扦插生根主要以诱导愈伤组织生根型为主。此外,还发现部分插穗只长出愈伤组织未生根,原因可能是个体差异或扦插时间还不够。也有研究表明,从愈伤组织到根原基的形成存在一个网络调控,不仅和生长素有关,过量的愈伤组织也会抑制根原基的形成[22-23]。
众所周知,古树扦插难生根,主要原因就是其年龄及其成熟度较高引起一系列内在结构与生理生化的变化[12-15],但哪些关键因素限制了其不定根的发生仍是一个世界性的难题。此外,课题组前期对古树扦插生根研究时还发现,材料的采集也是影响古树繁育的重要限制因素。本研究发现,50年生银杏扦插生根明显受枝龄影响,但不同枝龄如何影响不定根的形成,目前尚不清楚。植物体内的碳水化合物可分为结构性碳水化合物(SC)和NSC两大类[24],NSCs储存含量受到环境因素、营养条件等多方面的制约[25-26]。扦插早期在光合作用较弱的情况下, 不定根的形成主要依赖于插穗中储藏的NSC, 特别是插穗中的可溶性糖。本研究发现,不同枝龄茎段中总糖、葡萄糖、多糖和淀粉含量随着枝龄的升高逐渐降低(图 4),这与图 2中扦插生根能力随着枝龄升高而逐渐降低的趋势相吻合。然而,叶中NSC含量在不同枝龄中未有明显差异,这说明枝条年龄影响茎干NSC含量的变化,即枝龄越小的茎干中可用NSC越多,进而影响不定根的形成,这与许多研究认为碳水化合物含量高的插穗容易生根的报道一致[27-29]。研究还发现,树冠上、下部位对扦插生根影响较小,这与榉树、青海云杉、油橄榄、马尾松树冠下部枝条的扦插生根效果明显优于上部枝条的研究不一致[5-8]。本研究中,尽管叶中部多糖和总糖含量在树冠下部明显高于上部(图 3),但茎干NSC含量在树冠上部和下部无明显差异(图 4),这可能是扦插生根率在上下部位无明显差异的主要原因(图 2)。因此,本研究认为,茎干中NSC含量对扦插生根的影响远远大于叶中NSC含量的影响。此外,本研究中,500 mg·L-1IBA速蘸处理并未明显提高插穗生根率,今后还需根据不同部位和枝龄对生长素浓度进行优化。
-
本研究表明,银杏树冠上部和下部枝条对扦插生根无影响,但枝龄对不定根形成影响较大,枝龄越小生根率越高。未处理枝条的枝龄与生根率呈负相关,而茎段NSC含量与生根率呈正相关。叶片NSC含量是树冠下部高于上部,但在不同枝龄之间未见明显差异,表明叶片NSC含量对不定根形成影响较小。此外,银杏扦插生根过程可分为愈伤组织形成期、愈伤组织膨大期、不定根形成期、不定根伸长期4个阶段,不定根生成方式以愈伤生根类型为主,这为今后银杏扦插生根机制研究及古树繁育时插穗采集提供参考。
银杏枝条部位和年龄对不定根形成的影响及其与非结构碳水化合物含量的关系
Effects of Different Position and Ages of Twigs on Cutting of Ginkgo biloba and Its Relationship with Non-structural Carbohydrates
-
摘要:
目的 研究银杏枝条部位、年龄对不定根形成的影响,并探讨其相应的叶、茎段中非结构碳水化合物(NSC)含量变化与扦插生根的关系。 方法 以50年生银杏树冠上、下部枝条的1、2和3年生位置的茎段为材料截取插穗,500 mg·L-1 IBA与纯水对照处理基部60 s,在全光喷雾状态下研究扦插生根情况,并利用HLPC法分析相应部位叶和茎段中NSC含量。 结果 表明:银杏扦插不定根形成过程分为4个阶段,即0~4周愈伤形成期、4~6周愈伤膨大期、6~8周不定根开始形成期、8周后不定根伸长;生根部位主要在切口处。树冠上、下部位插穗的生根率未见明显差异,但随着枝龄的增加而明显降低。NSC分析表明:下部叶片NSC组分中多糖和总糖含量明显高于上部的,但茎段NSC的所有组分在上下部均无明显差异;随着枝龄的增加,相应位置叶片NSC各组分含量没有明显差异,但相应茎段NSC组分中葡萄糖、果糖、多糖、总糖、淀粉含量却明显降低,与生根率的变化趋势一致。此外,500 mg·L-1 IBA处理并未明显提高生根率,还需进一步优化处理浓度。 结论 银杏树冠上部和下部枝条对不定根形成无影响;未处理枝条的枝龄与生根率呈负相关,而茎段NSC含量与生根率呈正相关;叶片NSC含量对不定根形成影响较小;生根方式以愈伤生根类型为主。该结论将为今后银杏扦插生根及其机制研究提供参考。 Abstract:Objective To explore the effects of twig ages on the formation of the adventitious roots from the upper and lower branches in the crowns of Ginkgo biloba, and discuss the relationship between rooting and non-structural carbohydrates (NSC) in the corresponding leaves and stems. Method Experimental materials with the cutting of one-, two-, and three-year-old twigs were investigated from the upper and the lower parts of the crown, and the NSC contents were analyzed by the HLPC in the leaves and stems of the corresponding positions. All cuttings were treated with 0 and 500 mg·L-1 IBA under natural light and spraying management. Result The process of the adventitious root formation includes four stages:callus formation (0-4 weeks), callus expansion (4-6 weeks), initiation of adventitious root (6-8 weeks) and root elongation (after 8 weeks). No significant difference was observed in the rooting of cutting between the twigs from the upper and the lower branches of crowns, while it was considerably inhibited by the ages of twigs. The NSC analysis showed that the contents of polysaccharides and total sugars in the leaves from the lower crown were higher than the upper one, but all the NSC components tested showed no significant differences between the twigs from these two parts. However, the NSF contents had no significant changes in the corresponding leaves, whereas they decreased significantly in the corresponding stem fragments with the increasing ages of twigs, including glucose, fructose, polysaccharides, total sugars and starch, which showed the similar trends with the rooting changes. Besides, the treatment of 500 mg·L-1 IBA didn't improve the rooting rate compared to the control, and this needed to be further optimized. Conclusion The position of the upper and lower branches has no significant effect on the formation of adventitious roots in the crowns of G. biloba. The age of untreated twigs was negatively correlated with rooting, but stem NSC content was positively correlated with rooting; the induced callus rooting is the main type for the cutting of G. biloba. This result will provide the references for the future study of cutting process and its mechanism in G. biloba. -
Key words:
- Ginkgo biloba
- / cutting
- / adventitious roots
- / twig age
- / non-structural carbohydrates
-
表 1 银杏扦插不同生根类型的生根率
Table 1. Rooting rates of cutting rooting types in Ginkgo biloba
% 生根类型
Category树冠下部 Lower part of the crown 树冠下部 Lower part of the crown 1年生
Annual2年生
Biennial3年生
Triennial1年生
Annual2年生
Biennial3年生
Triennial切口生根 Rooting at the incision 55 45 42 47 39 30 皮部生根 Rooting at the skin 0 26 0 9 19 0 混合生根 Rooting at the skin and incision 18 9 31 5 10 22 愈伤未生根 Callus 27 21 27 38 31 48 注:各类型百分比指占总生根数量的百分比(%)。 -
[1] 王敏.国繁2号生根剂对银杏扦插效果的影响[J].山东农业大学学报:自然科学版, 2015, 46(1):57-60. [2] 徐萍, 张辉, 朱美弟, 等.银杏扦插繁殖技术[J].绿色科技, 2011(6):196-197. doi: 10.3969/j.issn.1674-9944.2011.06.086 [3] Marcio L, Aumond Jr, Artur T, et al. Events associated with early age-related decline in adventitious rooting competence of Eucalyptus globulus Labill[J]. Frontiers in Plant Science, 2017, 8:1734. doi: 10.3389/fpls.2017.01734 [4] 姜宗庆, 汤庚国, 肖文华, 等.不同处理对银杏嫩枝扦插生根及相关酶活性的影响[J].江苏农业科学, 2014, 42(5):162-164. doi: 10.3969/j.issn.1002-1302.2014.05.054 [5] 张俊叶.不同树冠部位和粗度插条对榉树扦插生根的影响[J].北方园艺, 2012(14):82-83. [6] 王军辉, 张建国, 张守攻, 等.青海云杉硬枝扦插的激素、年龄和位置效应研究[J].西北农林科技大学学报:自然科学版, 2006, 34(7):65-71. [7] 李子光, 王有兵, 严毅.插穗类型及生根剂处理时间对油橄榄扦插的影响[J].西部林业科学, 2015(4):154-157. [8] 季孔庶, 王章荣, 陈天华, 等.马尾松插穗生根能力变异的研究[J].南京林业大学学报:自然科学版, 1998, 22(3):66-70. [9] Hilo A, Shahinnia F, Druege U, et al. A specific role of iron in promoting meristematic cell division during adventitious root formation[J]. Journal of Experimental Botany, 2017, 68(15):4233-4247. doi: 10.1093/jxb/erx248 [10] Barraza A, Cabrera-Ponce J L, Gamboa-Becerra R, et al. The Phaseolus vulgaris PvTRX1h gene regulates plant hormone biosynthesis in embryogenic callus from common bean[J]. Frontiers in Plant Science, 2015, 6:577. [11] Gayler S, Grams T E E, Heller W, et al. A dynamical model of environmental effects on allocation to carbon-based secondary compounds in juvenile trees[J]. Annals of Botany, 2008, 101(8):1089-1098. [12] Day M E, Greenwood M S, Diaz-Sala C. Age-and size-related trends in woody plant shoot development:regulatory pathways and evidence for genetic control[J]. Tree Physiology, 2002, 22(8):507-513. doi: 10.1093/treephys/22.8.507 [13] Rutledge R G, Stewart D, Caron S, et al. Potential link between biotic defense activation and recalcitrance to induction of somatic embryogenesis in shoot primordia from adult trees of white spruce (Picea glauca)[J]. BMC Plant Biol, 2013, 13:116. doi: 10.1186/1471-2229-13-116 [14] 陈巧云.分关1号黄栀子不同枝龄扦插育苗及育苗成本分析[J].林业勘察设计, 2015(2):120-124. doi: 10.3969/j.issn.1004-2180.2015.02.028 [15] 李佳佳.霸王硬枝扦插繁殖技术研究[D].呼和浩特: 内蒙古农业大学, 2015. [16] Fattorini L, Veloccia A, Rovere F D, et al. Indole-3-butyric acid promotes adventitious rooting in Arabidopsis thaliana thin cell layers by conversion into indole-3-acetic acid and stimulation of anthranilate synthase activity[J]. BMC Plant Biology, 2017, 17(1):121. doi: 10.1186/s12870-017-1071-x [17] 王永格, 常卫民, 丛日晨.不同树龄银杏嫩枝扦插繁殖试验研究[J].科学技术与工程, 2012, 12(32):8642-8644. doi: 10.3969/j.issn.1671-1815.2012.32.033 [18] 刘福岭, 戴行钧.食品物理与化学分析方法[M].北京:轻工业出版社, 1987. [19] 于建国.现代实用仪器分析方法[M].北京:中国林业出版社, 1994. [20] 熊豫武, 周冬琴, 张垂胜.墨西哥柏嫩枝扦插繁殖试验[J].江苏农业科学, 2013, 41(1):165-166. doi: 10.3969/j.issn.1002-1302.2013.01.063 [21] 任高.银杏古树硬枝绿枝扦插试验分析[J].山西林业, 2014(5):47-48. doi: 10.3969/j.issn.1005-4707.2014.05.27 [22] Abu-Abied M, Rogovoy Stelmakh O, Mordehaev I, et al. Dissecting the contribution of microtubule behaviour in adventitious root induction[J]. Journal of Experimental Botany, 2015, 66(9):2813-2824. doi: 10.1093/jxb/erv097 [23] Druege U, Franken P, Hajirezaei M R. Plant hormone homeostasis, signaling, and function during adventitious root formation in cuttings[J]. Frontiers in Plant Science, 2016, 7:381. [24] 潘庆民, 韩兴国, 白永飞, 等.植物非结构性贮藏碳水化合物的生理生态学研究进展[J].植物学报, 2002, 19(1):30-38. doi: 10.3969/j.issn.1674-3466.2002.01.004 [25] 李娜妮, 何念鹏, 于贵瑞.中国东北典型森林生态系统植物叶片的非结构性碳水化合物研究[J].生态学报, 2016, 36(2):430-438. [26] Cernusak L A, Tcherkez G, Keitel C, et al. Why are non-photosynthetic tissues generally 13C enriched compared with leaves in C3 plants? Review and synthesis of current hypotheses[J]. Functional Plant Biology, 2009, 36(3):199-213. doi: 10.1071/FP08216 [27] 杨雪萌, 房伟民, 陈发棣, 等.两个菊花品种扦插生根过程及其插穗碳氮营养和内源激素的变化[J].南京农业大学学报, 2010, 33(4):19-24. [28] Kim J W, Kim T S. Rooting promotion in cuting propagation of tea[J]. Korean Journal of Medicinal Crop Science, 1995, 3(3):229-233. [29] Tombesi S, Palliotti A, Poni S, et al. Influence of light and shoot development stage on leaf photosynthesis and carbohydrate status during the adventitious root formation in cuttings of Corylus avellana L.[J]. Frontiers in Plant Science, 2015, 6:973. -




 下载:
下载: