-
土壤高盐是限制植物生长发育、地理分布的主要环境胁迫因子之一[1]。世界上有超过6%的土地被盐化,超过20%的灌溉土地遭受盐害[2-4]。盐生植物作为可以在盐化土壤中正常生存的一类植物,被广泛地用于盐碱地的生态改良和植被保护。因此,研究盐生植物的耐盐机制、发掘和选育耐盐植物对充分利用盐化土地、改善生态环境具有重要的生态和经济意义。
蒺藜科(Zygophyllaceae)白刺属(Nitraria)植物广泛生长在亚洲、非洲和欧洲盐碱地,因其较强的耐盐性,被应用于盐碱地的植被改善和生态环境改良。有关白刺耐盐的特性和生理生化机制研究已有一定的进展,研究报道白刺属可以耐受高达500 mmol·L−1的NaCl胁迫条件[5-6],NaCl胁迫可以显著增加 Na+ 浓度,降低 K+浓度[7]。有研究发现,在盐胁迫下,唐古特白刺(N. tangutorum)可能通过将Na+积聚在液泡内进行隔离,并对其它矿质营养离子进行选择性吸收,进而控制Na+/K+比值,以提高白刺耐盐性[8]。唐古特白刺幼苗经高盐处理7 d时,叶绿素含量随盐胁迫浓度升高而呈现先升后降的变化,当NaCl浓度达300 mmol·L−1时,叶绿素含量最高[9];盐胁迫也提高了游离脯氨酸、可溶性蛋白和可溶性糖等渗透调节物质的含量[10-12]。低浓度NaCl处理可以提高叶片中超氧化物岐化酶(SOD)、过氧化物酶(POD)和过氧化氢酶(CAT)等抗氧化酶活性,进而提高植物对盐分胁迫的适应性[13]。
关于白刺耐盐的分子机制研究可以归结为两个方面:一方面,在500 mmol·L−1 NaCl 高盐胁迫时,唐古特白刺幼苗体内涉及到的光合过程、氧化还原、逆境、防御、能量代谢、糖代谢、氨基酸代谢、信号转导、蛋白质合成、蛋白质折叠和装配、转录、膜运输、激素合成等途径的蛋白质表达发生了显著改变[4];另一方面,200 mmol·L−1 NaCl 中等盐胁迫诱导了比拉底白刺 (N. billardieri) 幼苗叶片内多条代谢途径的蛋白质表达水平的改变,其中涉及到的有碳水化合物代谢、光合过程、氨基酸代谢、蛋白质降解、蛋白质折叠和组装、蛋白质合成、氧化还原、次级代谢、信号转导、细胞周期、细胞骨架、细胞防御、能量代谢、膜与运输、转录调控等[14]。上述2个白刺研究均是通过蛋白质组学的方法,不同强度盐胁迫导致了一些相同类别蛋白质的表达及变化趋势,同时也呈现出一些细微的差别。
上述研究工作为了解白刺耐盐的生理生化与分子机制奠定了一定的基础,而基因作为植物应答环境胁迫的早期响应分子,对调控植株应对胁迫生存条件并适应胁迫环境起到关键作用。为了寻找白刺应答盐胁迫的基因并解析其分子机制,本研究以比拉底白刺幼苗为材料,运用转录组测序技术挖掘200 mmol·L−1 NaCl 胁迫下比拉底白刺幼苗叶片内的差异表达基因,并运用生物信息学方法分析差异表达基因的生物学功能及其参与的代谢途径。
-
比拉底白刺幼苗的培养参照Tian等[14]方法,并稍作调整。将经温水浸种24 h后的比拉底白刺种子播种于装有纯净河沙的塑料盆(高14 cm,直径12 cm,底部有孔),5个塑料盆放在一个塑料桶里(高15 cm,直径80 cm);然后放置在温室中培养,在(27± 2)℃下光照(400~800 μmol·m−2·s−1) 培养14 h和在(25±1)℃黑暗培养10 h,温室的相对湿度维持在60%~80%。待幼苗生长至2个月时,选取长势整齐的幼苗分为两组,第一组用200 mmol·L−1 NaCl处理,第二组为对照,每组3个重复。7 d时分别取样,放置于−80℃冰箱中保存备用。
-
取比拉底白刺幼苗叶片放于已灭过菌的研钵中,添加适量液氮快速研磨,然后取0.3 g 磨好的样品全部装入1mL EP 管中;加入1 mL Trizol 试剂,摇匀后静置10 min;加入0.3 mL氯仿,摇匀后静置10 min,然后离心15 min (4℃, 12 000 g) ;吸取上清液。再加入等体积异丙醇,静置4 h后离心15 min (4℃, 12 000 g) ;去上清液,并用75%酒精洗涤,然后同样在高速冷冻离心机上离心5 min (4℃, 12 000 g) ;用 75% 乙醇重复洗涤后,在冰上晾干;用无 RNAase 的水溶解后,分别用 1% RNA 琼脂糖凝胶电泳和 Nanodrop 仪检测 RNA 样品的质量和浓度。
-
总RNA经DNase I消化后,通过富集含有polyA尾巴的mRNA、mRNA打断成200 nt的小片段、反转录成第一条链cDNA、合成第二链cDNA等步骤,用 QIA quick PCR extraction kit 进行纯化,然后进行末端修复加 polyA。经回收纯化、PCR 富集获得 cDNA 文库。文库构建完成后,使用 Agilent 2100 Bioanalyzer和 ABI StepOnePlus Real-Time PCR System 分别对文库的插入片段长度和有效浓度进行检测,样品合格后在 Iilumina 测序平台 (Illumina HiSeqTM 2000) 进行高通量测序。将得到的序列原始文件 Raw Reads 进行过滤、比对、de novo组装、Unigene 功能注释、基因定量、差异基因筛选。其中,差异表达基因的筛选条件是 FDR (False Discovery Rate) <0.001 且基因表达差异倍数 (fold change) 大于2倍,选取这些基因作为应答盐胁迫的差异基因,用于后续分析。
-
利用 Blast2GO 软件将比对到 Gene Ontology 数据库中的所有差异基因进行 GO 功能注释和分类[15],网站是 http://www.geneontology.org/,获得转录本的GO 功能注释信息。
-
差异表达基因比对Gene Ontology数据库后,进行映射,得到目的GO条目(term)。以这些GO term为单位,通过超几何检验(phyper),得到检验p值,Bonferroni校正后,对于corrected p-value<0.05的GO term定义为在差异表达基因中显著富集的GO term。
-
将差异表达基因应用KEGG数据库预测其参与的代谢途径。以corrected p-value≤0.05为标准,筛选在差异表达基因中显著富集的代谢途径。
-
利用分子相互作用分析软件(STRING)和相互作用蛋白数据库(DIP)进行蛋白质相互作用网络预测,运用Cytoscape程序构建蛋白质相互作用网络[16]。
-
以分别提取的对照组及盐胁迫处理7d时的幼苗叶片RNA为模板,使用Takara公司的PrimeScriptTMRT reagent Kit with gDNA Eraser试剂盒反转录合成cDNA第一链作为实时荧光定量PCR (qRT-PCR) 反应的模板。从转录组数据中随机选择7个差异表达基因,利用 Primer 5.0 设计 qRT-PCR 引物,如表1。以18S rRNA 作为内参,引物为 5′-GCTGGATTTGCTGGTGGTAT-3′ 和 5′-TTCCTGGGTCTGTGCCTGT-3′ (表1)。使用 SYBR® Premix Ex TaqTM 荧光定量试剂盒进行荧光定量检测。每个样品进行3次重复,采用 2−ΔΔCt 计算相对表达量。
表 1 qRT-PCR引物序列
Table 1. Primers for qRT-PCR
Gene ID Forward primer Reverse primer comp83443_c0_seq9 GACCAAGACAACAGCGAGC CCATACCGACTAGGCAAACA comp75099_c0_seq1 CCGCCTTTCGTTGACACC GAAACAATGCTCGGCAAGAT comp71196_c0_seq2 GCTGTTACATTGCTTACTCATCG AACCTGAGGCACTTGGGATA comp71223_c0_seq1 CCAACCCAGATACCCATAACC TTGAGGACAAAATGAAGGAGC comp82053_c0_seq5 CATTTACGAGTGAAGGAGGTGAT GTGAATACATTGTCTCTCTGCGA comp82392_c1_seq3 TCATGCCTTCACGTATGCTTC CTTCTGGGACACTGACCGACT comp86989_c0_seq2 AGTTGCCATTCTCAAGTCCTAA TCCCCAAATCACGTCTTCTAG 18S rRNA GCTGGATTTGCTGGTGGTAT TTCCTGGGTCTGTGCCTGT -
以盐胁迫处理及对照组白刺叶片为材料,分别提取RNA后建立cDNA文库,用Illumina HiseqTM 2000测序。通过de novo拼接、组装后共获得168 463条unigenes。对测序获得的所有unigenes分别与COG、GO、KEGG、KOG、Pfam、Swiss-Prot、NR七大功能数据库进行比对和功能注释,注释率分别为21.5%、41.2%、14.2%、37.2%、42.4%、40.4%、59.7%(表2)。结果共注释到101 016条unigenes,占所有unigenes的60.0%,剩余67 447条(40.0%)unigenes未得到注释。在注释到的所有unigenes里,长度在300~1 000 bp的有24 329条,占24.1%;长度≥1 000 bp的有76 687条,占75.9%(表2) 。
表 2 Unigene在多个数据库中注释结果统计
Table 2. Statistics of annotation results in the databases
长度Length/bp COG GO KEGG KOG Pfam Swissprot NR 300≤长度Length<1 000 5 145 14 525 4 636 13 050 11 091 13 814 24 024 长度Length≥1 000 31 004 54 981 19 301 49 713 60 316 54 180 76 567 合计All Annotated 36 149 69 506 23 937 62 763 71 407 67 994 100 591 -
对盐胁迫处理及未处理对照的比拉底白刺幼苗叶片RNA-seq测序后得到的所有基因进行差异表达筛选,以log2 fold change (基因差异表达倍数)的绝对值>1且错配率FDR<0.001为差异表达基因(DEG)的筛选标准, 盐胁迫7 d时,共筛选得到差异表达基因196个,其中,79条DEGs在盐胁迫响应中上调表达,下调表达DEGs有117条。基因表达差异变化绝大部分集中在3倍左右,其中,comp73009_c0_seq1差异变化为−7.10,下调变化最大,该unigene注释为5′-甲基硫腺苷/s-腺苷同型半胱氨酸核苷酶(5′-methylthioadenosine/S-adenosylhomocysteine nucleosidase);comp79737_c1_seq2和comp82550_c1_seq4差异变化分别为5.29和5.21,上调变化最高,然而前者尚未得到注释,功能未知,后者注释为赤霉素调节蛋白(Gibberellin-regulated protein)。推测以上显著差异unigenes可能参与比拉底白刺的耐盐过程,需要进一步研究。
-
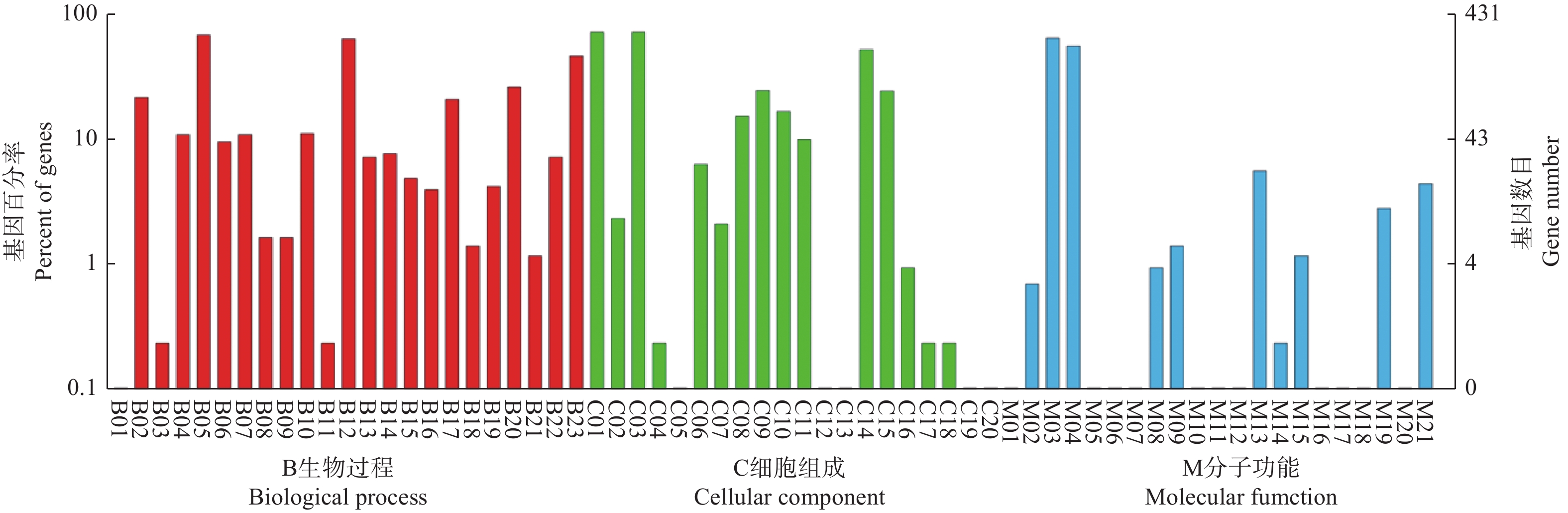
Gene Ontology(GO)分析能够比较全面地描述差异表达基因的主要生物学功能,是一个国际标准化的基因功能分类系统。对盐胁迫处理7 d的比拉底白刺叶片DEGs进行GO分析,划分为64个功能组(图1),GO数据库中的结构根据功能组的不同又进一步分为三类描述:生物学过程、分子功能和细胞组分图1显示了比拉底白刺盐胁迫后差异基因表达谱的总体情况。生物学过程主要集中在代谢过程、单体过程、细胞过程和刺激反应。在分子功能中,注释为结合和催化活性的差异基因最多,其次为转运活性和抗氧化活性。在细胞组分大类中,差异基因被注释到最多的亚类依次为细胞、细胞组分、细胞器、膜、细胞器组分和膜部分(图1)。以上注释较多的过程涉及到的基因可能参与了比拉底白刺的盐胁迫响应过程,进一步挖掘这些差异表达基因有助于研究其抗逆机制和品质改良。
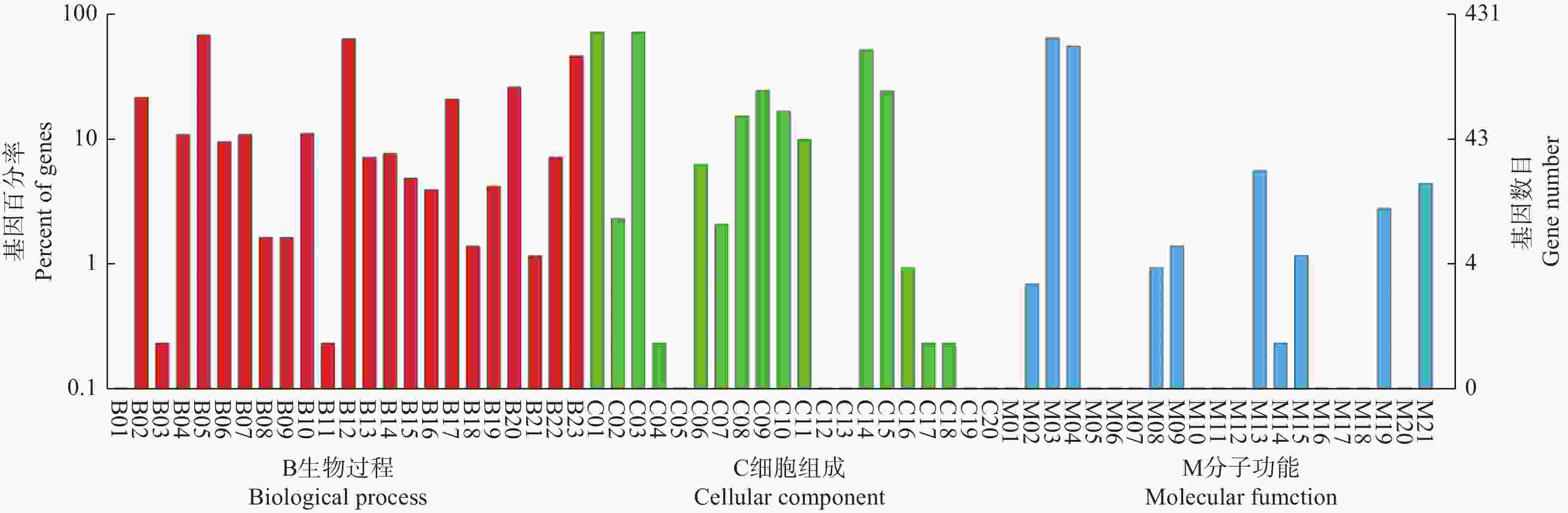
图 1 盐胁迫下比拉底白刺叶片差异表达基因的GO功能聚类注释图
Figure 1. Gene Ontology classification annotation of differentially expressed genes in the leaves of N. billardieri under salt stress
通过进一步对比拉底白刺叶片DEGs的GO富集分析(校正后p-value<0.05)发现:在生物学过程中DEGs富集最显著的GO term分别是细胞壁高分子分解代谢过程、几丁质分解代谢过程、多糖分解代谢过程、氨基糖代谢过程、防御反应。在细胞组分中,富集最显著的GO term分别是液泡、叶绿体类囊体膜、细胞外区域、质外体、细胞壁。在分子功能中的DEGs富集最显著的GO term分别是几丁质结合、几丁质酶活性、氧化还原酶活性、醌结合、血红素结合。
-
在生物体中,基于通路的分析有助于进一步了解基因的生物学功能和上下游基因的相互作用,深入理解基因与功能的关系。本文使用KEGG功能富集分析盐胁迫处理7 d时比拉底白刺幼苗叶片的差异表达基因可能涉及的代谢通路,发现比拉底白刺响应盐胁迫的DEGs涉及到25条KEGG代谢通路(图2),其中,碳水化合物代谢过程的差异基因最多,占14%,其次为运输和分解代谢,占9%;蛋白质折叠、分类、降解和其它次级代谢产物的生物合成均占7%,免疫应答系统占6%,氨基酸代谢和信号转导分别占5%和4%。与盐胁迫应答相关的环境适应占2%(图2)。KEGG分析可以从功能的角度聚焦到通路及基因,也可以从基因的角度锁定功能和互作关系,直观地显示了比拉底白刺在盐胁迫下差异表达基因的代谢过程和信号通路,有助于更好地研究比拉底白刺响应盐胁迫的分子机制。
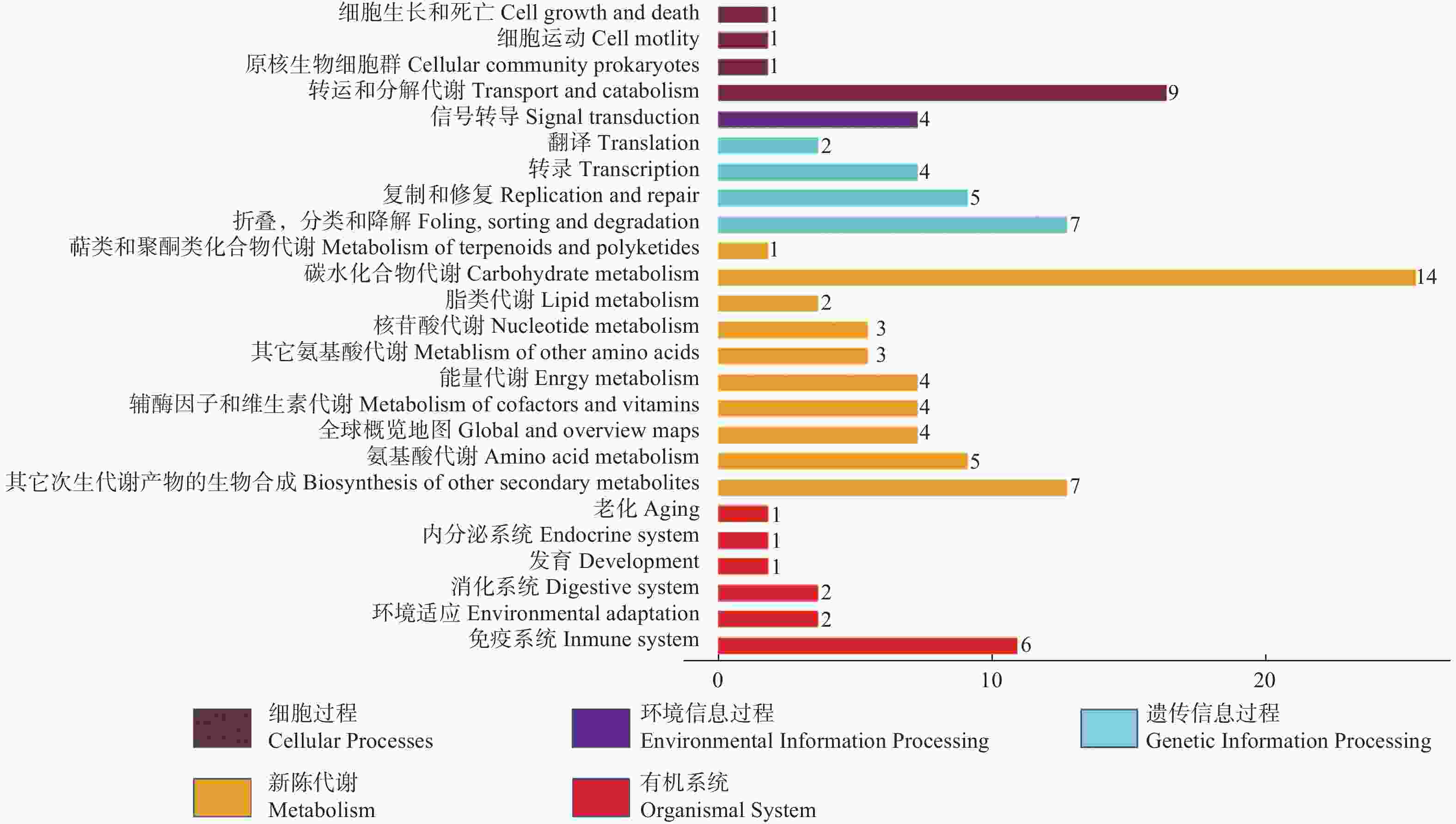
图 2 盐胁迫下比拉底白刺叶片差异表达基因的KEGG通路分析
Figure 2. KEGG pathway analysis of differentially expressed genes in the leaves of N. billardieri under salt stress
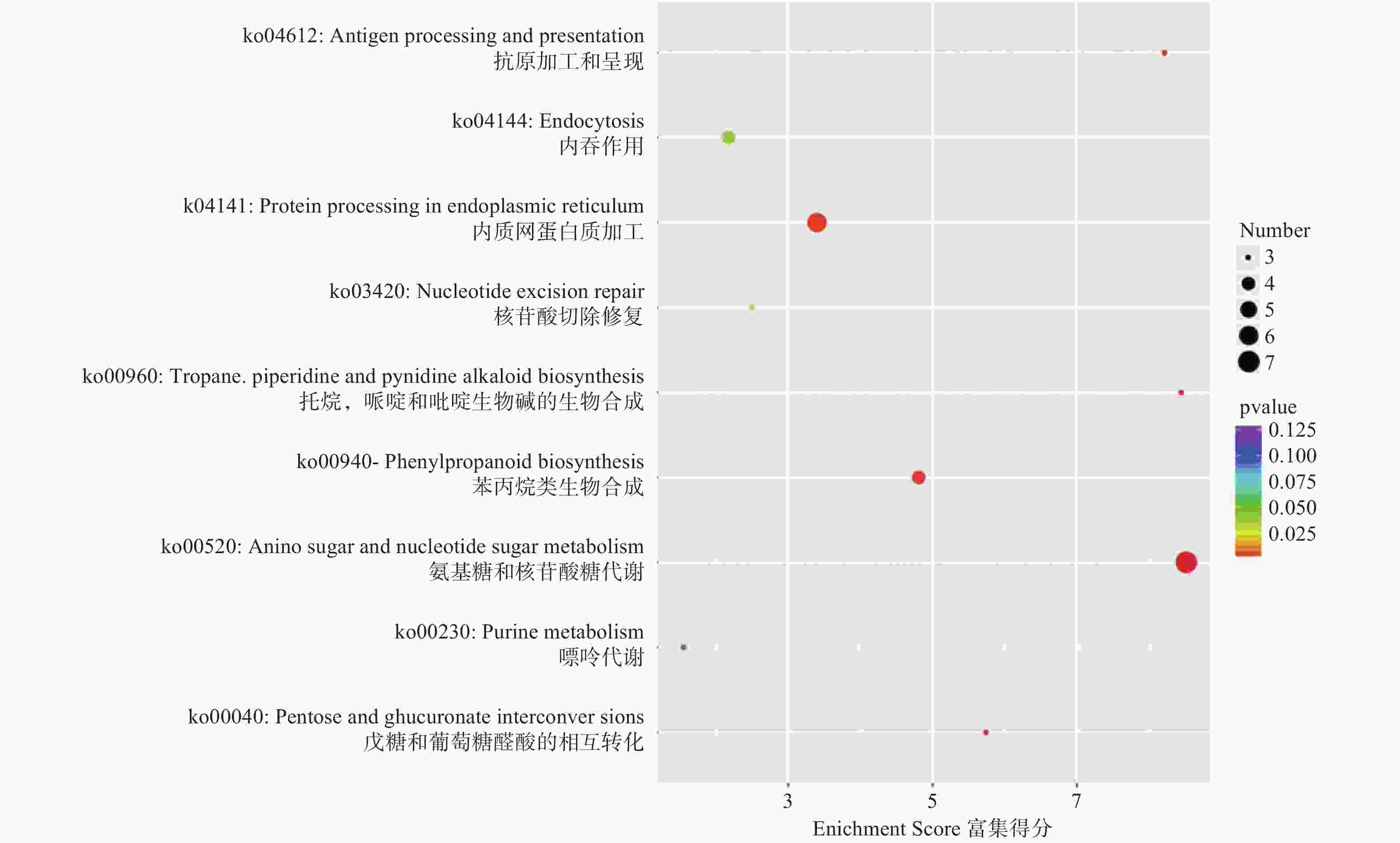
以校正后p-value<0.05为筛选阈值,盐胁迫7 d比拉底白刺叶片差异表达基因的KEGG富集分析发现,有9条代谢途径产生显著变化(图3),分别是苯丙烷类生物合成、氨基糖和核苷酸糖代谢、托烷,哌啶和吡啶生物碱的生物合成、抗原加工和呈现、内质网中的蛋白质加工、核苷酸切除修复、戊糖和葡萄糖醛酸的相互转化、内吞作用、嘌呤代谢(图3)。以上9条代谢通路有助于获得比拉底白刺在抵御盐胁迫时的代谢信息,以便更清楚地理解其在盐胁迫应答中的过程。
-
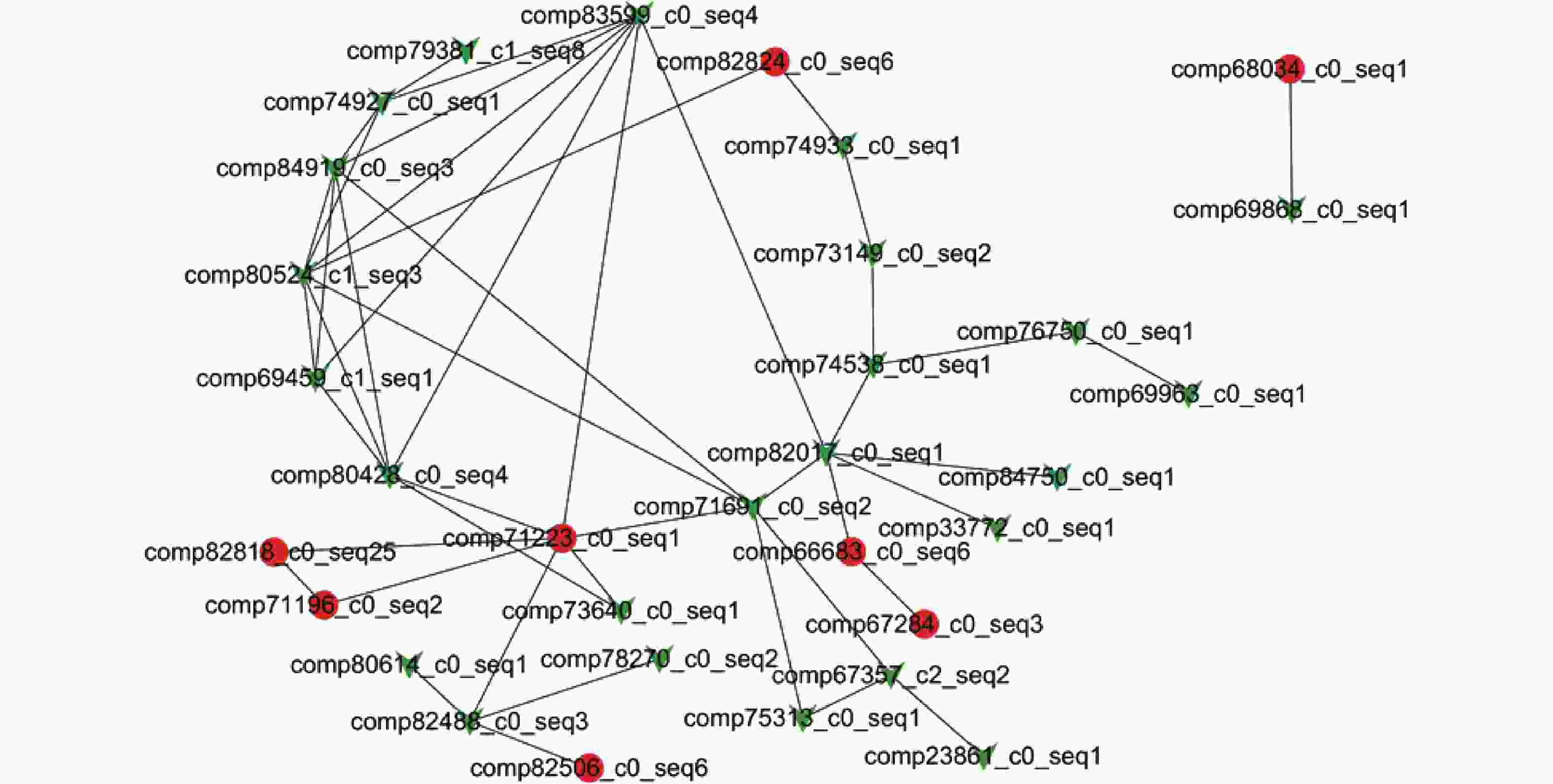
为了研究比拉底白刺幼苗是如何通过基因之间的相互作用来传递盐胁迫信号,通过String数据库和搜索软件构建了盐应答基因在细胞内的互作网络(图4、表3)。在基因作用网络中检测到一组相互作用的基因簇,共包含32个基因(图4)。组成相互作用网络的这些基因主要与信号转导、氧化还原平衡、蛋白质合成、蛋白质折叠和组装、蛋白质降解、转录调控、次级代谢、细胞拯救/防御等途径相关。转录调控和氧化还原平衡在基因相互作用网络中占据着重要位置,它们可能在比拉底白刺幼苗响应盐胁迫反应中起重要作用。此外,基因comp71223_c0_seq1、基因comp83599_c0_seq4和基因comp71691_c0_seq2,作为节点,占据了网络的中心位置。
表 3 盐胁迫诱导的基因相互作用网络中差异表达基因的名称及注释
Table 3. The name and annotation of differentially expressed genes responding to salt stress in gene interaction network analysis
基因 gene 基因注释 gene annotation 基因 gene 基因注释 gene annotation comp71223_c0_seq1 Heat shock cognate 70 kDa protein comp82824_c0_seq6 1-aminocyclopropane-1-carboxylate oxidase comp82506_c0_seq6 Protein LNK4 comp74538_c0_seq1 Glycerophosphodiester phosphodiesterase GDE1 comp71691_c0_seq2 Win-like protein comp73640_c0_seq1 Galactinol synthase 2 comp80524_c1_seq3 Flavanone 3-dioxygenase comp67284_c0_seq3 Putative branched-chain-amino-acid aminotransferase comp69868_c0_seq1 Cysteine proteinase 15A comp79381_c1_seq8 Bidirectional sugar transporter SWEET1a comp80428_c0_seq4 Calreticulin-1 comp71196_c0_seq2 Ferredoxin comp74933_c0_seq1 1-aminocyclopropane-1-carboxylate oxidase homolog comp68034_c0_seq1 Non-specific lipid-transfer protein 1 comp84919_c0_seq3 Probable WRKY transcription factor 41 comp69459_c1_seq1 NAC transcription factor NAM-B2 comp83599_c0_seq4 L-type lectin-domain containing receptor kinase IV.1 comp73149_c0_seq2 Monoacylglycerol lipase comp75313_c0_seq1 Peroxidase 4 comp74927_c0_seq1 Ammonium transporter 1 member 2 comp82017_c0_seq1 DNA damage-repair/toleration protein DRT100 comp80614_c0_seq1 9-cis-epoxycarotenoid dioxygenase NCED2, chloroplastic comp84750_c0_seq1 Pectinesterase 1 comp69963_c0_seq1 Wound-induced protein 1 comp82818_c0_seq25 Carboxyl-terminal-processing peptidase 3, chloroplastic comp23861_c0_seq1 Wound-induced proteinase inhibitor 1 comp82488_c0_seq3 Chlorophyllide a oxygenase, chloroplastic comp66683_c0_seq6 Tropinone reductase homolog At2g30670 comp76750_c0_seq1 -- comp33772_c0_seq1 G-type lectin S-receptor-like serine/threonine-protein kinase comp67357_c2_seq2 Protein NP24 comp78270_c0_seq2 Acetamidase -
为了验证RNA-Seq数据的准确性,随机选择7个差异表达基因,取对照和盐胁迫7 d的比拉底白刺叶片进行qRT-PCR实验。结果显示:这7个基因在qRT-PCR的结果与转录组分析的趋势一致(图5),而在表达变幅倍数上有些许差异,可能是由于两类实验的检测灵敏度及数据分析方法不同造成的。盐胁迫处理前后,7个差异基因的表达特征与测序结果呈现相同的变化趋势,验证了转录组测序结果的可靠性。
-
本研究进行了多次预实验,通过观察盐胁迫下植株的表型发现,盐生植物比拉底白刺在7 d时开始出现叶片轻微卷曲的现象,之后开始逐渐萎蔫,到9 d时萎蔫症状较明显。相对于非盐生植物,盐生植物能够耐受一定强度的盐胁迫环境一段时间,在一定盐浓度范围的土壤环境下正常生长[17-18]。为了研究比拉底白刺应答盐胁迫的分子机制,本实验选择在其表型性状刚开始出现时进行取样和转录组测序分析,以便更好地理解盐生植物特有的耐盐机制。
植物盐胁迫是一个由多个基因参与表达调控的作用网络,转录组提供了基因的多样性、表达水平差异以及时空变化,利用转录组测序技术的实用性和高效性可以促进植物响应非生物逆境胁迫的分子机制研究[19-20]。本研究采用Illumina HiseqTM 2000高通量测序技术对盐胁迫7 d与未做处理的比拉底白刺幼苗叶片进行了转录组分析,共获得了168 463条unigenes,与七大数据库的注释率达60.0%,注释结果较好,大部分基因功能得到注释,与泡泡刺(N. sphaerocarpa)的注释率(62.1%)接近[21]。剩余67 447条(40.0%)unigenes未得到注释,可能是比拉底白刺中的新基因。
植物中各类转录因子对于调控各种诱导型基因的表达以及植物生长发育、适应环境等起主要作用[22]。该研究筛选出的差异基因中涉及到了WRKY转录因子(comp85183_c0_seq4、comp85183_c0_seq10、comp74597_c0_seq1)、乙烯响应转录因子(comp82253_c0_seq3)、NAC转录因子(comp69459_c1_seq1)、GATA转录因子(comp74878_c0_seq4)、发病机制相关转录因子(comp83152_c0_seq5),这些unigenes在盐胁迫下均有显著响应,其中,WRKY转录因子具有高度保守的WRKY结构域,研究表明能够参与损伤、衰老、发育、抗病等抗逆反应[23]。乙烯响应转录因子(ERF)家族属于AP2/ERF超转录因子家族,具有保守的一个AP2/ERF结构域,在植物生长发育、环境应答反应(干旱、低温、高盐、病虫害等胁迫)中具有重要作用[24]。本研究发现的几个转录因子需要进一步挖掘其功能,以期为探究比拉底白刺的耐盐机理作出贡献。
通过盐胁迫诱导的差异表达基因GO分析结果可见,盐胁迫主要引起了比拉底白刺叶片内与代谢过程、环境刺激应答、防御反应等有关的生物学过程变化,以及与催化活性、结合活性、转运活性和抗氧化活性有关的分子功能的变化,这与比拉底白刺在蛋白质水平上对盐胁迫的应答模式有些类似[14]。初步表明,比拉底白刺在受到低盐胁迫时,可能通过合成或者降解一些蛋白酶类,改变蛋白质结构和含量,以抵抗低盐逆境。
从比拉底白刺幼苗叶片差异表达基因参与的代谢途径可见,盐胁迫主要引起了白刺幼苗叶片内与碳水化合物、氨基酸代谢相关的基因表达发生变化,同时也诱导了与蛋白质折叠、分类和降解相关的基因表达发生改变,这可能与盐胁迫导致了幼苗叶片内一些蛋白质代谢变化相关[4, 14]。比拉底白刺幼苗叶片在受到低盐逆境胁迫时,氨基酸和核苷酸糖代谢途径有显著富集,可能其光合作用也受到一定影响,碳水化合物代谢活跃,推测其可能通过减少物质合成,控制能量代谢来抵抗低盐环境[25]。由盐胁迫引起的植株叶片表型的轻微变化可能是由于差异表达基因所参与的代谢途径的改变引起的,正是由于植株体内代谢途径的改变引起了诸如光合作用、质膜渗透力等生理现象的变化,进而导致表型的变化[4, 14]。
将比拉底白刺幼苗叶片响应盐应答差异基因在细胞内构建互作网络,作为网络中的“hubs”(连接到许多其他的蛋白质)和“bottlenecks”(在一个网络的子网络的关键连接器),如基因comp71223_c0_seq1注释为热激同源蛋白(Heat shock cognate 70 kDa protein),基因comp83599_c0_seq4注释为L型凝集素域受体激酶(L-type lectin-domain containing receptor kinase IV.1),和基因comp71691_c0_seq2注释为Win类蛋白(Win-like protein),它们占据了网络的中心位置,可能在白刺幼苗叶片对盐胁迫处理的响应过程中发挥重要作用。因此,通过基因相互作用网络分析可以初步了解这些基因在比拉底白刺响应盐胁迫过程中起的作用,互作关系有待进一步研究。
-
本研究通过对盐胁迫 7 d 与未处理的比拉底白刺叶片进行转录组测序及相关生物信息学分析,共获得168 463条 unigenes ,筛选到196条差异表达基因。通过GO 功能和 KEGG 通路分析,理清了差异表达基因富集的分子功能与代谢通路。此外,进一步构建了差异基因互作网络,得到了重要的节点基因。综上所述,本研究为挖掘和找寻重要耐盐候选基因提供了参考,同时为研究比拉底白刺响应盐胁迫的分子机制,以及为下一步培育比拉底白刺耐盐新品种奠定了基础。
盐胁迫下比拉底白刺差异表达基因的转录组分析
Transcriptome Analysis of Differentially Expressed Genes of Nitraria billardieri Under Salt Stress
-
摘要:
目的 为了挖掘比拉底白刺耐盐相关基因,对其盐胁迫下差异表达基因进行筛选分析。 方法 以比拉底白刺幼苗为材料,用 200 mmol·L-1 NaCl 对幼苗处理7 d,并对胁迫处理和对照植株叶片进行转录组测序及生物信息学分析。 结果 有效序列组装共得到应答盐胁迫的168 463条 unigenes 和196个差异表达基因。通过差异基因 GO 和 KEGG 功能聚类,分别获得64个 GO 功能小类和25条 KEGG 通路。进一步基因相互作用网络分析发现,转录调控、氧化还原以及抗逆相关基因在比拉底白刺应答盐胁迫中发挥重要作用,其中,筛选到3个重要的节点基因,分别是热激同源蛋白基因、L 型凝集素类受体激酶基因和 Win 类蛋白基因。 结论 本研究获得了盐胁迫下比拉底白刺的差异表达基因及功能注释信息,有助于理解其耐盐的分子机制,为后续开发耐盐分子标记及通过基因编辑改良植物耐盐特性提供了科学依据。 Abstract:Objective To find the salinity tolerance genes of Nitraria billardieri, the differentially expressed genes (DEGs) under salt stress were selected and analyzed . Method The seedlings of N. billardieri were subjected to salt stress treatments with 200 mmol·L-1 NaCl for 7 days. High-throughput RNA-seq technology was used to generate the transcriptome of salt-treated leaves and the control, and the related bioinformatics analysis was performed. Result A total of 168 463 unigenes and 196 DEGs responding to salt stress were obtained with clean reads assembled. 64 subclasses and 25 KEGG pathways were enriched in the GO and KEGG annotation, respectively. Further gene interaction network analysis revealed that the genes related to transcriptional regulation, redox and stress tolerance play important roles in the response to salt stress of N. billardieri. Three key node genes were screened out: heat shock cognate 70 kDa protein gene, L-type lectin-domain containing receptor kinase IV.1 gene and Win-like protein gene. Conclusion In this study, the DEGs of N . billardieri under salt stress and the functional annotations were obtained. It will be helpful to understand the molecular mechanism of salt tolerance of N. billardieri. It also provide scientific basis for the subsequent development of salt-tolerance molecular markers and the improvement of salt-tolerance characteristics in plants through gene editing. -
表 1 qRT-PCR引物序列
Table 1. Primers for qRT-PCR
Gene ID Forward primer Reverse primer comp83443_c0_seq9 GACCAAGACAACAGCGAGC CCATACCGACTAGGCAAACA comp75099_c0_seq1 CCGCCTTTCGTTGACACC GAAACAATGCTCGGCAAGAT comp71196_c0_seq2 GCTGTTACATTGCTTACTCATCG AACCTGAGGCACTTGGGATA comp71223_c0_seq1 CCAACCCAGATACCCATAACC TTGAGGACAAAATGAAGGAGC comp82053_c0_seq5 CATTTACGAGTGAAGGAGGTGAT GTGAATACATTGTCTCTCTGCGA comp82392_c1_seq3 TCATGCCTTCACGTATGCTTC CTTCTGGGACACTGACCGACT comp86989_c0_seq2 AGTTGCCATTCTCAAGTCCTAA TCCCCAAATCACGTCTTCTAG 18S rRNA GCTGGATTTGCTGGTGGTAT TTCCTGGGTCTGTGCCTGT 表 2 Unigene在多个数据库中注释结果统计
Table 2. Statistics of annotation results in the databases
长度Length/bp COG GO KEGG KOG Pfam Swissprot NR 300≤长度Length<1 000 5 145 14 525 4 636 13 050 11 091 13 814 24 024 长度Length≥1 000 31 004 54 981 19 301 49 713 60 316 54 180 76 567 合计All Annotated 36 149 69 506 23 937 62 763 71 407 67 994 100 591 表 3 盐胁迫诱导的基因相互作用网络中差异表达基因的名称及注释
Table 3. The name and annotation of differentially expressed genes responding to salt stress in gene interaction network analysis
基因 gene 基因注释 gene annotation 基因 gene 基因注释 gene annotation comp71223_c0_seq1 Heat shock cognate 70 kDa protein comp82824_c0_seq6 1-aminocyclopropane-1-carboxylate oxidase comp82506_c0_seq6 Protein LNK4 comp74538_c0_seq1 Glycerophosphodiester phosphodiesterase GDE1 comp71691_c0_seq2 Win-like protein comp73640_c0_seq1 Galactinol synthase 2 comp80524_c1_seq3 Flavanone 3-dioxygenase comp67284_c0_seq3 Putative branched-chain-amino-acid aminotransferase comp69868_c0_seq1 Cysteine proteinase 15A comp79381_c1_seq8 Bidirectional sugar transporter SWEET1a comp80428_c0_seq4 Calreticulin-1 comp71196_c0_seq2 Ferredoxin comp74933_c0_seq1 1-aminocyclopropane-1-carboxylate oxidase homolog comp68034_c0_seq1 Non-specific lipid-transfer protein 1 comp84919_c0_seq3 Probable WRKY transcription factor 41 comp69459_c1_seq1 NAC transcription factor NAM-B2 comp83599_c0_seq4 L-type lectin-domain containing receptor kinase IV.1 comp73149_c0_seq2 Monoacylglycerol lipase comp75313_c0_seq1 Peroxidase 4 comp74927_c0_seq1 Ammonium transporter 1 member 2 comp82017_c0_seq1 DNA damage-repair/toleration protein DRT100 comp80614_c0_seq1 9-cis-epoxycarotenoid dioxygenase NCED2, chloroplastic comp84750_c0_seq1 Pectinesterase 1 comp69963_c0_seq1 Wound-induced protein 1 comp82818_c0_seq25 Carboxyl-terminal-processing peptidase 3, chloroplastic comp23861_c0_seq1 Wound-induced proteinase inhibitor 1 comp82488_c0_seq3 Chlorophyllide a oxygenase, chloroplastic comp66683_c0_seq6 Tropinone reductase homolog At2g30670 comp76750_c0_seq1 -- comp33772_c0_seq1 G-type lectin S-receptor-like serine/threonine-protein kinase comp67357_c2_seq2 Protein NP24 comp78270_c0_seq2 Acetamidase -
[1] Stepien P, Johnson G. N. Contrasting responses of photosynthesis to salt stress in the glycophyte Arabidopsis and the halophyte thellungiella: Role of the plastid terminal oxidase as an alternative electron sink[J]. Plant Physiology, 2009, 149(2): 1154-1165. doi: 10.1104/pp.108.132407 [2] Zhu J K. Plant salt tolerance[J]. Trends in Plant Science, 2001, 6(2): 66-71. doi: 10.1016/S1360-1385(00)01838-0 [3] Munns R, Tester M. Mechanisms of salinity tolerance[J]. Annual Review of Plant Biology, 2008, 59(1): 651-681. doi: 10.1146/annurev.arplant.59.032607.092911 [4] Cheng T L, Chen J H, Zhang J B, et al. Physiological and proteomic analyses of leaves from the halophyte Tangut Nitraria reveals diverse response pathways critical for high salinity tolerance[J]. Frontiers in Plant Science, 2015, 6: 30. [5] 杨 升, 张华新, 刘 涛. 16个树种盐胁迫下的生长表现和生理特性[J]. 浙江农林大学学报, 2012, 29(5):744-754. doi: 10.11833/j.issn.2095-0756.2012.05.018 [6] 张 雪, 贺康宁, 史常青, 等. 盐胁迫对柽柳和白刺幼苗生长与生理特性的影响[J]. 西北农林科技大学学报: 自然科学版, 2017, 45(1):105-111. [7] 闫永庆, 袁晓婷, 刘 威, 等. 盐胁迫及外源Ca2+对白刺离子吸收、运输的影响[J]. 东北农业大学学报, 2014, 45(3):71-78. doi: 10.3969/j.issn.1005-9369.2014.03.013 [8] 杨秀艳, 张华新, 张 丽, 等. NaCl胁迫对唐古特白刺幼苗生长及离子吸收、运输与分配的影响[J]. 林业科学, 2013, 49(9):7-9. [9] 闫永庆, 高彦博, 刘 威, 等. 外源Ca2+对盐胁迫下唐古特白刺光合作用影响[J]. 东北农业大学学报, 2016, 47(4):57-64. doi: 10.3969/j.issn.1005-9369.2016.04.008 [10] 范小峰, 杨颖丽, 程转霞. NaCl胁迫下唐古特白刺愈伤组织生理生化变化研究[J]. 干旱地区农业研究, 2009, 27(3):3-5. [11] 倪建伟, 武 香, 张华新, 等. 3种白刺耐盐性的对比分析[J]. 林业科学研究, 2012, 25(1):48-53. doi: 10.3969/j.issn.1001-1498.2012.01.009 [12] 左凤月, 郝秀芬, 陈占峰, 等. 小果白刺和泡果白刺的耐盐性[J]. 天津农学院学报, 2013(2):11-14. doi: 10.3969/j.issn.1008-5394.2013.02.004 [13] 鲁 艳, 雷加强, 曾凡江, 等. NaCl胁迫对大果白刺幼苗生长和抗逆生理特性的影响[J]. 应用生态学报, 2014, 25(3):711-717. [14] Tian L, Zhu L M, Cheng T L, et al. Physiological and protein responses in leaves of Nitraria billardieri seedlings to moderate salt stress[J]. Journal of Plant Interactions, 2018, 13: 522-531. doi: 10.1080/17429145.2018.1526979 [15] Conesa A, Gotz S. Blast2GO: a comprehensive suite for functional analysis in plant genomics[J]. International Journal of Plant Genomics, 2008, 2008: 1-12. [16] Franceschini A, Szklarczyk D, Frankild S, et al. STRING v9.1: Protein-protein interaction networks, with increased coverage and integration[J]. Nucleic Acids Research, 2013, 41: 808-815. [17] Ding M, Hou P, Shen X, et al. Salt-induced expression of genes related to Na+/K+ and ROS homeostasis in leaves of salt-resistant and salt-sensitive poplar species[J]. Plant Molecular Biology, 2010, 73: 251-269. doi: 10.1007/s11103-010-9612-9 [18] Liu Q, Tang J, Wang W, et al. Transcriptome analysis reveals complex response of the medicinal/ ornamental halophyte Iris halophila Pall. to high environmental salinity[J]. Ecotoxicology and Environmental Safety, 2018, 165: 250-260. doi: 10.1016/j.ecoenv.2018.09.003 [19] 孙瑞芬, 张艳芳, 郭树春, 等. 基于RNA-Seq技术的盐胁迫向日葵转录组信息分析[J]. 分子植物育种, 2015, 13(12):2736-2742. [20] Agarwal P K, Gupta K, Lopato S, et al. Dehydration responsive element binding transcription factors and their applications for the engineering of stress tolerance[J]. Journal of Experimental Botany, 2017, 68: 2135-2148. doi: 10.1093/jxb/erx118 [21] 马 婧, 邓 楠, 褚建民, 等. 泡泡刺高通量转录组鉴定及其黄酮类代谢途径初步分析[J]. 林业科学研究, 2016, 29(1):61-66. doi: 10.3969/j.issn.1001-1498.2016.01.009 [22] 赵 航, 贾富强, 张富春, 等. 盐胁迫下盐穗木差异表达基因的转录组信息分析[J]. 生物信息学, 2014, 12(2):90-98. doi: 10.3969/j.issn.1672-5565.2014.02.03 [23] Shi W Y, Du Y T, Ma J, et al. The WRKY transcription factor GmWRKY12 confers drought and salt tolerance in soybean[J]. International Journal of Molecular Sciences, 2018, 19: 4087. doi: 10.3390/ijms19124087 [24] 张计育, 王庆菊, 郭忠仁. 植物AP2/ERF类转录因子研究进展[J]. 遗传, 2012, 34(7):835-847. [25] Qin D D, Wu H Y, Peng H R, et al. Heat stress-responsive transcriptome analysis in heat susceptible and tolerant wheat (Triticum aestivum L.) by using Wheat Genome Array[J]. BMC Genomics, 2008, 9: 432. doi: 10.1186/1471-2164-9-432 -




 下载:
下载: