-
世界各地的生物博物馆保存有数百万个标本,其包含了时间和空间上不同历史阶段广泛的生物群,提供了生物多样性的丰富记录[1-2],是生物分类学、生物地理学和生物系统学研究的重要组成部分[3-7]。同时,博物馆标本为物种进化研究提供了难以置信的潜力[8],历史标本与现生标本的结合可以揭示物种在一定时间尺度上以响应环境压力在表现型或基因型上发生的变化[9-10]。随着分子生物学、基因组学以及相关统计工具的发展,标本中更多的分子数据正在被挖掘和利用,例如对博物馆标本中基因序列的分析能够标识目前形成的物种遗传多样性的过程[11];将从模式标本获得的序列作为新物种描述和分类修订的附加数据来源,可增加物种识别的准确性并加快物种分类的过程等[12-13]。然而,标本中低浓度和小片段的DNA限制了从其中获得基因序列的能力[14-15]。因此,前人做了很多关于标本DNA提取方法的研究[16-19]。Guzman-Larralde et al[19]评价了DNeasy®Blood& Tissue Kit、改良DNeasy®Blood& Tissue Kit、CaCl2法、改良CaCl2法和HotSHOT法5种方法对乙醇保存昆虫标本的DNA提取效果。魏亦寒等[20]用了4种方法(CTAB法、SDS法、磁珠法以及GeneJET基因组DNA纯化试剂盒)对扶桑绵粉蚧成虫的新鲜样本以及乙醇保存标本进行DNA的分离提取,并对4种方法的DNA提取效果进行了比较分析。Hunter等人[21]在提取双翅目昆虫标本的DNA时将裂解液用超声波处理。虽然在国内外期刊上已经发表了很多有关标本DNA提取方法的相关文献,但是目前为止还未有一个适用于各类型标本的、提取效果较好的通用方法。标本DNA的提取方法常因保存方法、物种体型大小以及保存物种的不同而存在差异[22-27]。因此为了保证顺利从标本中提取到分子数据并减少标本资源的浪费,常需要根据标本的保存方法、保存物种以及标本体型大小等选择合适的DNA提取方法。因此本研究尝试比较分析SDS法、磁珠法以及E.Z.N.A.™昆虫DNA提取试剂盒3种方法对舞毒蛾新鲜样本、干燥成虫标本和福尔马林幼虫标本的DNA提取效果,以确定适用于3种类型标本的DNA提取方法,为进行下一步的实验打好基础。
此外,标本的保存时间、保存方式以及保存环境常会对标本的DNA降解产生影响[14-15, 28-30],从而导致从标本中扩增基因序列变得困难。Zimmermann 等人[29]表明鳞翅目夜蛾科标本保存时间越久,标本中含有的大片段DNA越少,PCR扩增成功率越低。Strange等人[14]在利用熊蜂(Bombus)标本扩增微卫星位点时,同样表明微卫星位点扩增的成功率与标本的保存时间成负相关。Sutrisno等人[30]在利用鳞翅目通用引物进行基因扩增时发现:对于保存时间低于6年的标本可以成功扩增出650 bp的片段;保存7年的标本扩增300 bp的片段较容易成功;而对于保存7~19年的标本未扩增得到目的片段。季清娥等[31]比较并分析了茧蜂的冷冻标本、干燥标本和乙醇标本的DNA降解情况,结果表明50 mmol·L−1无水乙醇保存的寄生蜂标本DNA降解程度最低。Miller等人[15]利用酒精保存蜘蛛标本并调查了保存时间、体型大小、系统发育距离等因素对DNA条形码测序成功率的影响。结果表明保存时间与测序成功率成负相关;标本大小与测序成功率成正相关,与较小的蜘蛛物种相比可以从保存更长时间的较大的蜘蛛物种获得标准DNA条形码序列;而物种系统发育距离与测序成功率无明显的相关关系。通过比较不同类型标本的基因序列扩增成功率不仅能够预测是否能够从保存标本中成功获取到分子数据以及进一步的研究,而且能够为标本的处理和保存提供指导。因此本研究尝试分析讨论保存时间和保存方式对舞毒蛾标本基因序列扩增成功率的影响,从而为舞毒蛾标本的保存和处理提供建议。
-
新鲜舞毒蛾幼虫样本由中国林业科学研究院昆虫病毒研究中心提供。舞毒蛾的卵块是2008年在辽宁收集,然后在温室中进行人工饲养,饲养条件如下:温度保持在24~26°C,光周期保持14L:10D,相对湿度60%~80%。
在中国林业科学研究院森林生物标本馆中,本研究获得了1956年至1996年收集的舞毒蛾标本(表1),所有标本都保存在低温(10 ℃左右)、通风、光线暗的环境中。标本在保存时间和保存方式上存在差异,因此本研究尝试利用标本进行两个方面的研究:一方面利用1956年、1979年和1993年收集的干燥成虫标本和福尔马林幼虫标本以及新鲜舞毒蛾幼虫样本分析并比较不同DNA提取方法对各标本的提取效果,以确定一种适合各标本DNA提取的最优方法;另一方面利用本研究中确定的最优DNA提取方法提取其他所有舞毒蛾标本的DNA,并将提取的标本DNA作为模板进行PCR扩增,分析并比较保存时间和保存方式对基因序列扩增的影响。
表 1 本研究所用的舞毒蛾标本
Table 1. Lymantria dispar specimens used in this study
收集地点Collection locality 收集年份Collected year 保存方法Type of preservation 样本数量Number of samples 黑龙江Heilongjiang 1956 干燥成虫dried adult 6 内蒙古Inner Mongolia 1956 福尔马林幼虫formalin larva 5 河北Hebei 1964 干燥成虫dried adult 5 黑龙江Heilongjiang 1979 干燥成虫dried adult 5 辽宁Liaoning 1979 福尔马林幼虫formalin larva 5 北京Beijing 1982 干燥成虫dried adult 5 北京Beijing 1987 干燥成虫dried adult 6 四川Sichuan 1993 干燥成虫dried adult 5 四川Sichuan 1993 福尔马林幼虫formalin larva 10 USA, Newark, DE 1996 干燥成虫dried adult 8 辽宁Liaoning 2018 新鲜幼虫fresh larva 8 注:新鲜样本标注的是提取时间。
Note: the extraction time of fresh samples is recorded. -
以往的研究表明SDS法[20, 32]和磁珠法[18, 33]对各种标本的DNA提取效果较好,另外E.Z.N.A.TM昆虫DNA提取试剂盒是一种专用于提取昆虫DNA的试剂盒,因此本研究首先比较了这3种方法对舞毒蛾标本的DNA提取效果。
-
(1)干燥标本的预处理 :干燥标本DNA提取前先用干净的毛刷刷掉标本表面的鳞毛、灰尘等污染物,然后取适当组织先用0.9% NaCl溶液浸泡3 h[18],然后将浸泡后的组织用去离子水清洗3~4次,组织清洗后在室温条件下(15~25 ℃)自然风干,最后用液氮研磨至粉末状。一般取成虫标本腹部组织30 mg进行DNA提取。
(2)福尔马林标本的预处理:福尔马林标本在DNA提取前需利用不同浓度的乙醇溶液逐步将福尔马林置换出来[17, 34-35]。本试验依次用浓度为65%、70%、75%、80%、85%、90%、95%和100%的乙醇溶液置换。在预处理过程中先用低浓度乙醇溶液浸泡标本2 h,浸泡后5 000×g离心10 min,丢弃浸泡液,然后再依次用高浓度乙醇溶液浸泡标本2 h,浸泡后5 000×g离心10 min,丢弃浸泡液。用各浓度乙醇溶液浸泡离心后再用去离子水清洗3~4次,自然风干后剪去头部取30 mg组织利用全自动样品快速研磨机(净信JXFSTPRP-64)以60 Hz的频率研磨1 min。
另外,新鲜的幼虫标本在进行DNA提取前用去离子水清洗3~4次,组织清洗后在室温条件下(15~25 ℃)自然风干,自然风干后剪去头部取30 mg组织利用全自动样品快速研磨机(净信JXFSTPRP-64)以60 Hz的频率研磨1 min。
-
根据曲良建等[32]的SDS-蛋白酶K法对预处理过的标本进行DNA的提取,但本试验中为减少裂解液对核酸的损伤,将组织、裂解液、蛋白酶K的混合液65 ℃恒温水浴2 h。
-
磁珠法动物基因组DNA抽提试剂盒购买自生工生物工程(上海)股份有限公司,根据操作说明对预处理过的标本分别进行提取。
(1)将研磨过的组织放入1.5 mL离心管中,加入400 μLBuffer MACL、200 μLBuffer MCL和20 μLProteinase K,震荡混匀,然后65 ℃恒温水浴2 h,水浴过程中每隔0.5 h混匀一次以充分裂解组织细胞。
(2)其他操作步骤参考蒋欣悦[35]的研究。
-
E.Z.N.A.™昆虫DNA提取试剂盒购买自上海索莱宝生物科技有限公司,根据操作说明对预处理过的标本分别进行提取。
(1)将研磨过的组织放入1.5 mL 离心管中,在离心管中加入350 μL Buffer CTL和25 μL Proteinaseine K(20 mg·mL−1),然后60 ℃恒温水浴2 h,水浴过程中每隔0.5 h混匀一次以充分裂解组织细胞。
(2)水浴裂解后,在2 mL离心管中加入350 μL核酸提取液(氯仿:异戊醇=24∶1),震荡混匀后10 000×g离心5 min,离心后取250 μL上清液小心转移至新的1.5 mL离心管中。在上清液中加入5 μLRNase A(25 mg·mL−1)溶液,混匀,室温放置10~15 min。
(3)1.5 mL离心管中加入250 μLBuffer CBL,震荡混匀15 s,然后60 ℃恒温水浴10 min。
(4)1.5 mL离心管中加入250 μL无水乙醇(96%~100%),震荡混匀15 s。
(5)将HiBind®DNA吸附柱放入新的2 mL收集管中,将1.5 mL离心管中的750 μL混合液转移至吸附柱中,10 000×g离心1 min,丢掉收集管中的废弃液并将吸附柱重新放入2 mL收集管中。
(6)吸附柱中加入500 μLBuffer HB,10 000×g离心1 min,丢掉废弃液及收集管并将吸附柱放入新的2 mL收集管中。
(7)吸附柱中加入700 μLWash Buffer(使用前需要加入无水乙醇),10 000×g离心1 min,丢掉废弃液及收集管并将吸附柱放入新的2 mL收集管中。
(8)吸附柱中加入700 μLWash Buffer(使用前需要加入无水乙醇),10 000×g离心1 min,丢掉收集管中的废弃液,将吸附柱放回2 mL收集管中然后10 000×g离心2 min,丢掉废弃液及收集管。
(9)将吸附柱放入新的1.5 mL离心管中,加入50~100 μLElution Buffer(提前60~70 ℃恒温水浴5 min)并在60 ℃恒温水浴2 min,最后10 000×g离心1 min得到DNA提取液。
将3种方法提取的标本DNA用超微量紫外可见分光光度计(DeNovixDS-11)测定浓度和纯度,将已知浓度和纯度的DNA置于-20 ℃低温保存备用。此外,取部分已经测定浓度和纯度的DNA样本送去厚泽生物公司,利用Qsep100全自动核酸蛋白质分析系统检测样本中的DNA片段分布情况。一般情况下待检测的样本DNA浓度需高于10 ng·μL−1,DNA纯度(A260/A280)需在1.8~2.0之间。对于DNA提取浓度较高(>500 ng·μL−1)的样本,为保证检测结果的准确性,检测之前常需要用Elution Buffer稀释,稀释后浓度在100 ng·μL−1左右最好。
在比较不同DNA提取方法对各标本的提取效果时,本研究仅利用了1956年、1979年和1993年收集的干燥成虫标本和福尔马林幼虫标本进行分析。在确定一种适合各标本DNA提取的最优方法后,本研究利用最优DNA提取方法提取其他舞毒蛾标本的DNA,并将提取的所有标本DNA作为模板进行PCR扩增,分析保存时间和保存方式对基因序列扩增的影响。
-
本研究检测到所有标本的DNA片段大小都分布在20 bp至900 bp之间,而且全自动核酸蛋白质分析系统自动将所有DNA片段依次分成了44组(20~40 bp, 40~60 bp,
$\cdots $ , 880~900 bp),并提供了每组DNA片段在所有片段中所占的百分比。本研究首先利用似然比检验(Likelihood ratio test, LRT)分析不同方法提取的标本DNA中各组DNA片段百分比分布的差异,以确定在DNA提取过程中3种方法对DNA的损伤情况,其中每一个样本的数据都由44组DNA片段组成,同一种标本所有样本的各组DNA片段所占的百分比被平均。在SPSS 18.0软件中进行LRT检验时参数的设置如下所示:(1)在加权个案窗口选择加权个案,频率变量输入各组DNA片段的百分比;(2)在交叉表窗口的“行”输入44组DNA片段的分布情况(20~40 bp, 40~60 bp,$\cdots $ , 880~900 bp),“列”输入标本类型;(3)统计量选择卡方;(4)在单元格窗口依次选择观察值、期望值、行、列和无调节。此外,为了直观表现出不同标本DNA降解程度的差异,本研究将所有原始DNA片段百分比分布的数据导入到Origin 9.5软件中以获得DNA片段百分比分布的拟合曲线。在进行曲线拟合时,本研究首先将原始数据导入Origin 9.5软件中以获得DNA片段分布的散点图,其中44组DNA片段作为横坐标,每组DNA片段所占有的百分比作为纵坐标,然后对散点图进行了各种非线性拟合以获得最佳拟合曲线(具有最高相关系数R2)。为了直观表现出干燥成虫标本和福尔马林标本的DNA片段分布差异,本研究利用Origin 9.5软件制作了两种标本的堆积柱形图。由于44组DNA片段所占的百分比相对较小,若直接用44组DNA片段所占的百分比作图会导致堆积柱形图对比不清晰。因此,在制作堆积柱形图时本研究将44组DNA片段分成了四个大组(A,B,C和D),其中A组包括第1至8组的DNA片段,B组包括第9至17组的DNA片段,C组包括第18至26组的DNA片段,D组包括第27至第44组的DNA片段,然后分别计算这四组DNA片段在所有片段中各自所占百分比。最后利用四组DNA片段在所有片段中各自所占百分比在Origin 9.5软件中绘制两种标本成组堆积柱状图。在绘制拟合曲线和堆积柱状图时,本研究利用了每一种标本所有样本的各组DNA片段百分比的平均值。 -
本研究根据标本中的DNA片段分布情况(20~900 bp)设计了15对COI基因特异性引物,其目标片段在216 bp至977 bp之间。在设计引物时参考了GenBank上已经公布的舞毒蛾完整的线粒体基因序列(FJ617240,KY798442和KY923059-KY923067)。所有设计引物信息如表2所示。
表 2 本研究所用的引物
Table 2. All primers used in this study
引物名称Primers name 引物方向Direction 核苷酸序列5′-3′Nucleotide sequence 5′-3′ 长度Length/bp 退火温度Anneal temperatures/℃ Lco 1 F GCATGAGCTGTAACAATAG 216 49.6 R CAATTTATCGCTTAAACTCAGCC Lco 2 F CCAATTACCAAATCCTCC 274 48.0 R CAATTTATCGCTTAAACTCAGCC Lco 3 F GGATAATCCTTTATGAATGGGG 285 51.0 R CGACGATACTCTGATTACCCAG Lco 4 F CCTGAAAATAGTGGATATCAGTG 303 54.3 R CACGAGCTTACTTTACCTCTGC Lco 5 F GGGGGAAAAGAGCAATTCGTTG 320 52.3 R CGTTCTTTCTATAGGAGCAG Lco 6 F GGGAAATTATTCAAATCCTGG 357 49.6 R GCTCATGGAGGTAGATCTGTTG Lco 7 F CCAGCTAAGTGAAGAGAAA 386 48.0 R ATCAGGAATAGTGGGAAC Lco 8 F TTTTTCCTCTTTCTTGGG 420 48.5 R GGATGAACTGTTTACCCTC Lco 9 F GGGTAATCAGAGTATCGTCG 477 48.5 R TTATTGTTTGGGCTCACCAC Lco 10 F TGGTGAGCCCAAACAATAAA 516 48.5 R AAAATGGAGCAGGAACAGGA Lco 11 F GCAGGGTCAAAAAAGGAT 557 48.5 R TCGAGCTGAATTAGGGAA Lco 12 F TCAGAGAATAGAAGGTGAGT 670 48.5 R TTGTAGAAAATGGAGCAG Lco 13 F CCTAATCTTCAGAGAATAGAAGGTGAGT 766 52.0 R GGAGCCCCTGATATAGCTTTCCCCCG Lco 14 F CCTGAAAATAGTGGATATCAGTG 845 48.5 R TGGAGCAGGAACAGGA Lco 15 F GGGTAATCAGAGTATCGTCG 977 48.5 R AGAAAATGGAGCAGGAACAG 将已知浓度和纯度的DNA作为模板,利用以上15对引物进行PCR扩增,扩增体系为:DNA模板质量<1 μg,2×Tap PCR MasterMix(天根)12.5 μL,正反引物各1 μL,ddH2O补至25 μL。PCR反应循环的设置为:
94℃ 3 min 94℃ 3 sec 48 ℃~54.3 ℃ 30 sec (2~4步) 30个循环 72 ℃ 1 min 72 ℃ 5 min
其中15对特异性引物的退火温度不同,在PCR扩增时具体退火温度的设置如表2所示。
将扩增产物上样到1%的琼脂糖凝胶中,以DL2000 DNA Marker(天根)作为参考DNA Marker,在1×TAE电泳缓冲液中电泳30~40 min,电泳完成后取出琼脂糖凝胶在凝胶成像系统中检测PCR扩增结果。
-
3种提取方法提取的各标本的DNA浓度和纯度如表3所示,从表中可以看出SDS法对1956年、1979年和1993年收集干燥成虫标本和福尔马林幼虫标本的DNA提取效果相对较差,特别是未能从1956年收集的福尔马林标本中提取到DNA;磁珠法和E.Z.N.A.TM昆虫DNA提取试剂盒对于新鲜样本的提取效果差异不是很明显,但E.Z.N.A.TM昆虫DNA提取试剂盒对于干燥标本和福尔马林标本的DNA提取浓度和纯度都较磁珠法较好。
表 3 不同方法提取DNA的浓度与纯度
Table 3. The concentration and purity of genomic DNA extracted by different methods
SDS法
SDS method磁珠法
Magnetic bead method昆虫DNA提取试剂盒
Insect DNA Kit收集时间
Collected yearDNA浓度/
DNA concentration/(ng·μL−1)A260/A280 DNA浓度
DNA concentration/(ng·μL−1)A260/A280 DNA浓度
DNA concentration/(ng·μL−1)A260/A280 干燥成虫
Dried adult1956 124.569 1.592 198.471 2.013 297.778 1.817 福尔马林幼虫
Formalin larval1956 — — 13.172 1.752 15.099 1.823 干燥成虫
Dried adult1979 146.203 1.645 183.012 1.965 298.682 1.795 福尔马林幼虫
Formalin larval1979 12.181 2.276 15.191 1.892 19.164 1.850 干燥成虫
Dried adult1993 143.643 1.541 212.776 1.874 309.136 1.802 福尔马林幼虫
Formalin larval1993 15.704 2.103 22.903 1.896 28.193 1.834 新鲜活体
Fresh sample2018 208.994 1.647 445.383 1.842 451.766 1.853 注:表中数据为每种标本所有样本的DNA浓度与纯度的平均值。
Note: DNA concentration and purity of all samples per specimen are averaged. -
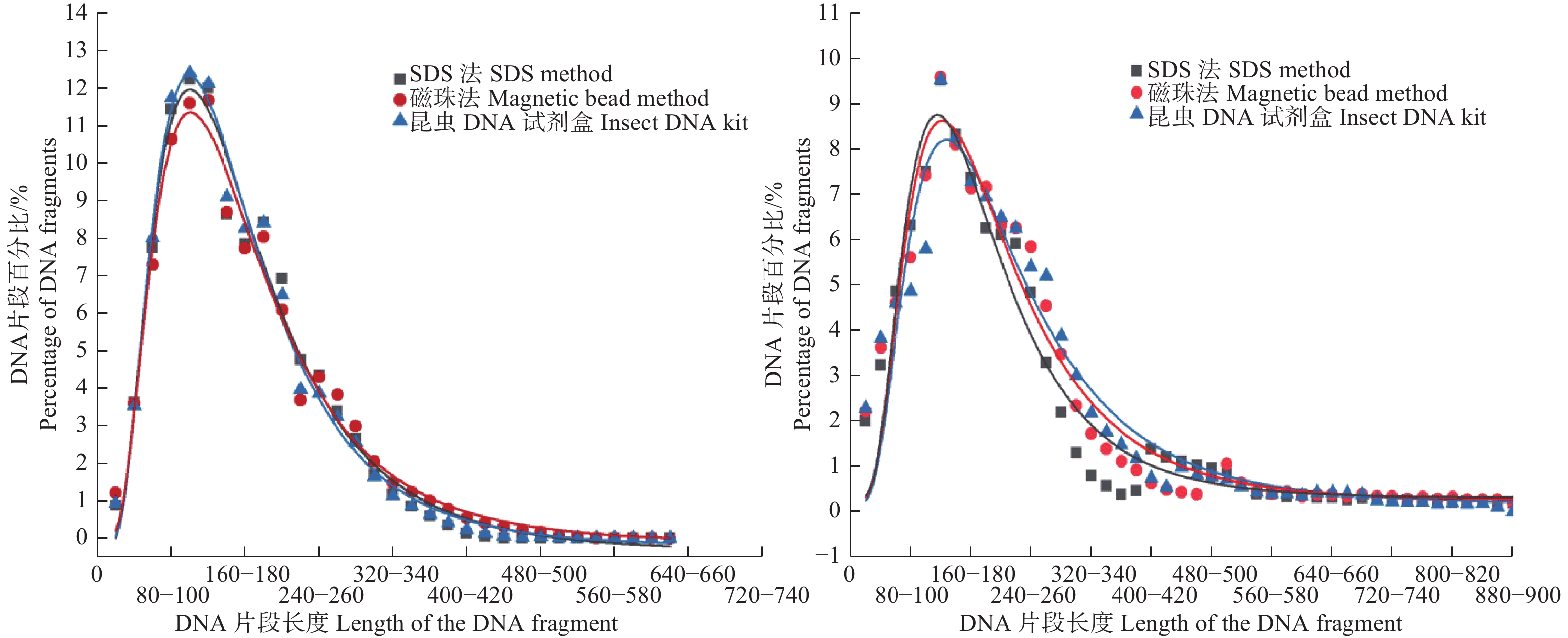
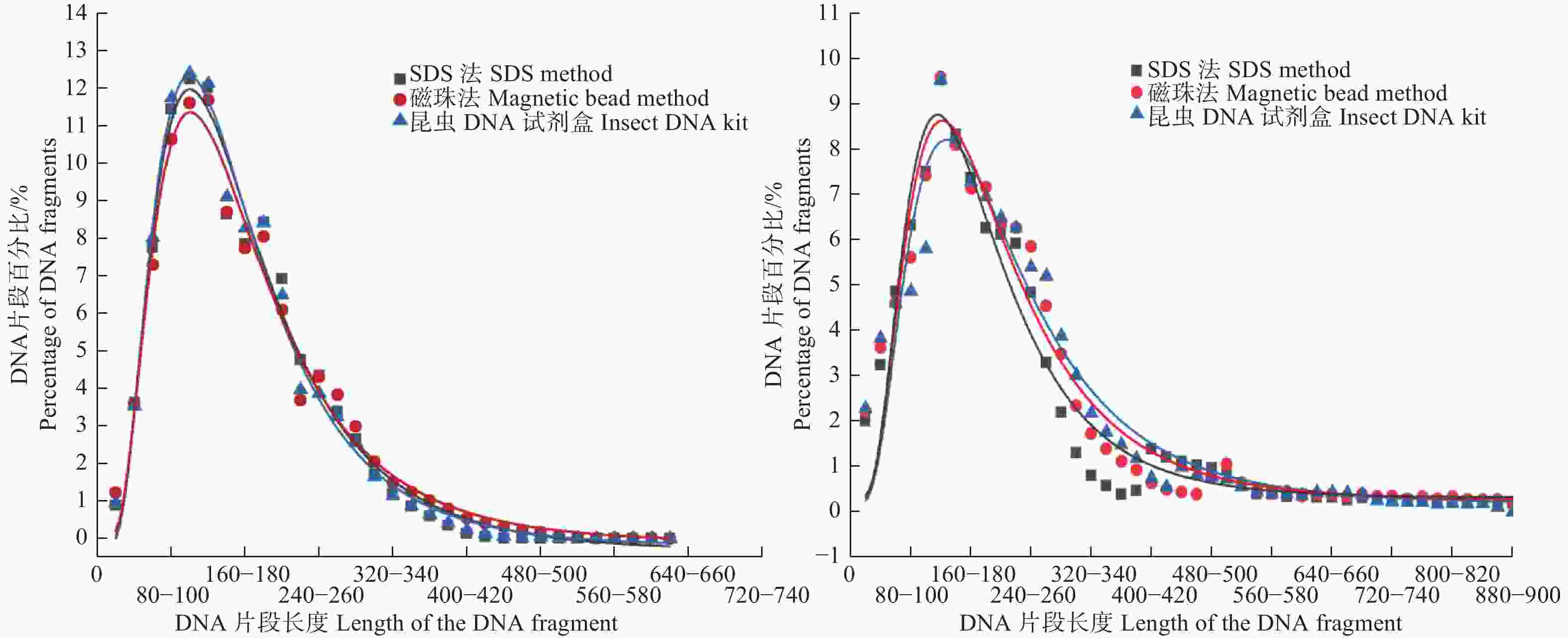
本研究对用不同方法提取的干燥成虫标本(收集时间相同)的DNA片段分布进行了似然比检验,结果发现用不同方法提取的干燥成虫标本(收集时间相同)的DNA片段分布差异是不显著的(df=1, P1956=0.745, P1979=0.560, P1993=0.101)。同样的,通过对用不同方法提取的福尔马林幼虫标本(收集时间相同)的DNA片段分布进行似然比检验,发现用不同方法提取的福尔马林幼虫标本(收集时间相同)的DNA片段分布差异是不显著的(df=1, P1956=0.439, P1979=0.983, P1993=0.482)。因此,本研究表明虽然3种DNA提取方法的提取效果存在差异,但是3种方法在提取过程中都未对标本DNA产生损伤,也可能3种方法在提取过程中对标本DNA产生的损伤程度是相同的。此外,本研究获得了不同方法提取的干燥成虫标本和福尔马林幼虫标本(收集时间相同)的DNA片段百分比分布的拟合曲线,如图1所示。从图1中可以看出不同方法提取的干燥成虫标本和福尔马林幼虫标本的(收集时间相同)DNA片段分布的拟合曲线基本是一致,这同样表明3种提取方法在提取过程中对标本DNA的损伤程度差异是不明显的。
-
各年份收集的舞毒蛾标本的15对引物的扩增结果如图2所示,从图2中可以看出干燥标本的保存时间越久长序列目的片段的扩增越困难。对于1982年之前保存的标本未能扩增出大于400 bp的基因序列,而对于1987年到1996年收集的标本扩增大于400 bp基因序列的成功率显著增加。但是所有保存标本均未能扩增获得大于600 bp的目的片段,而15对引物在新鲜舞毒蛾样本中均扩增成功。本研究推测导致所有标本均未能扩增获得大于600 bp的目的片段的原因主要与标本DNA的降解有关,而且标本保存时间越长(22~62 a)舞毒蛾标本提取DNA的降解越严重。本研究获得了各年份收集的舞毒蛾干燥标本的DNA片段百分比分布的拟合曲线,如图3所示。从图3可以看出不同年份收集的舞毒蛾干燥标本的DNA片段百分比分布的拟合曲线明显不一致。随着保存时间的增加,标本中大片段DNA所占的百分比明显降低,小片段DNA所占的百分比显著增加。
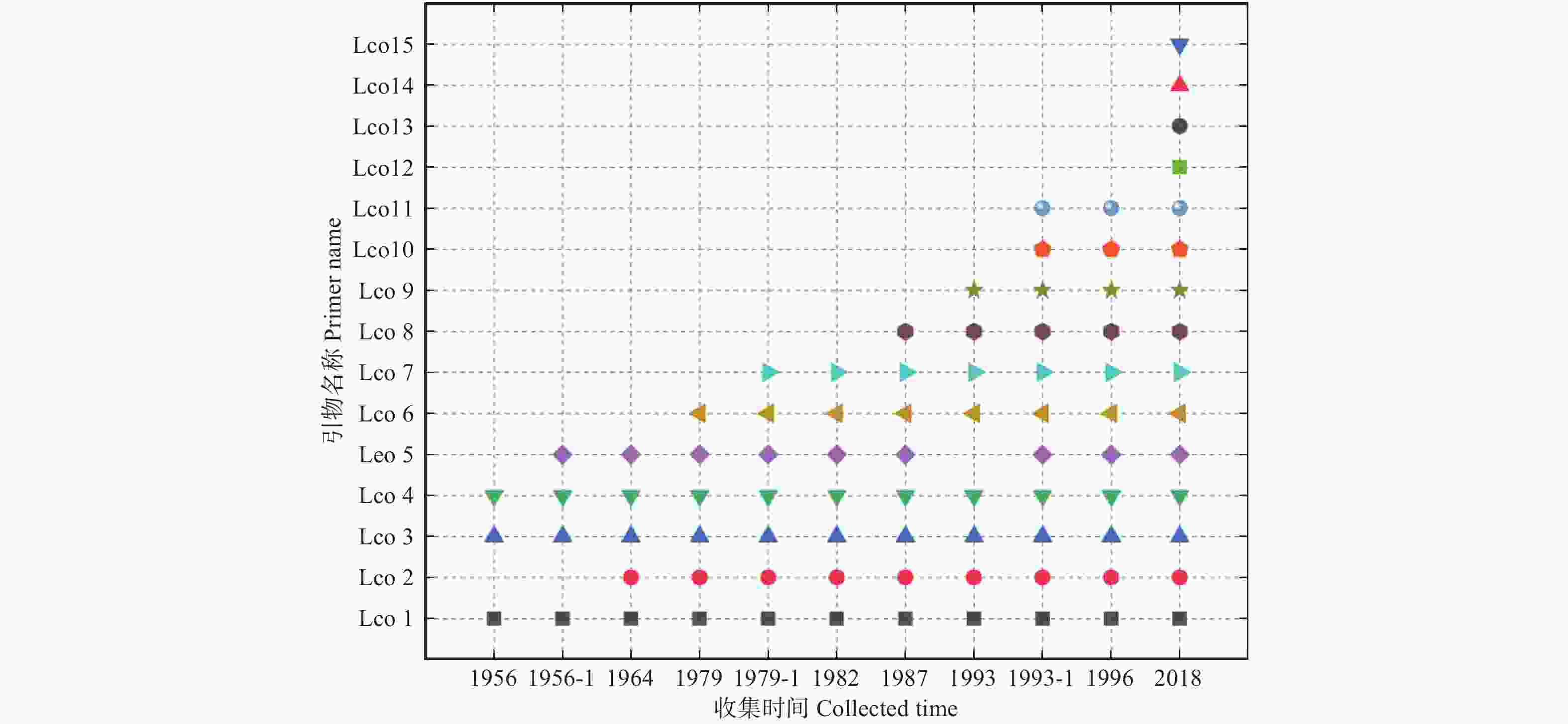
图 2 不同年份收集的舞毒蛾标本的测序成功情况
Figure 2. Sequencing success profile for L. dispar specimens collected in different years
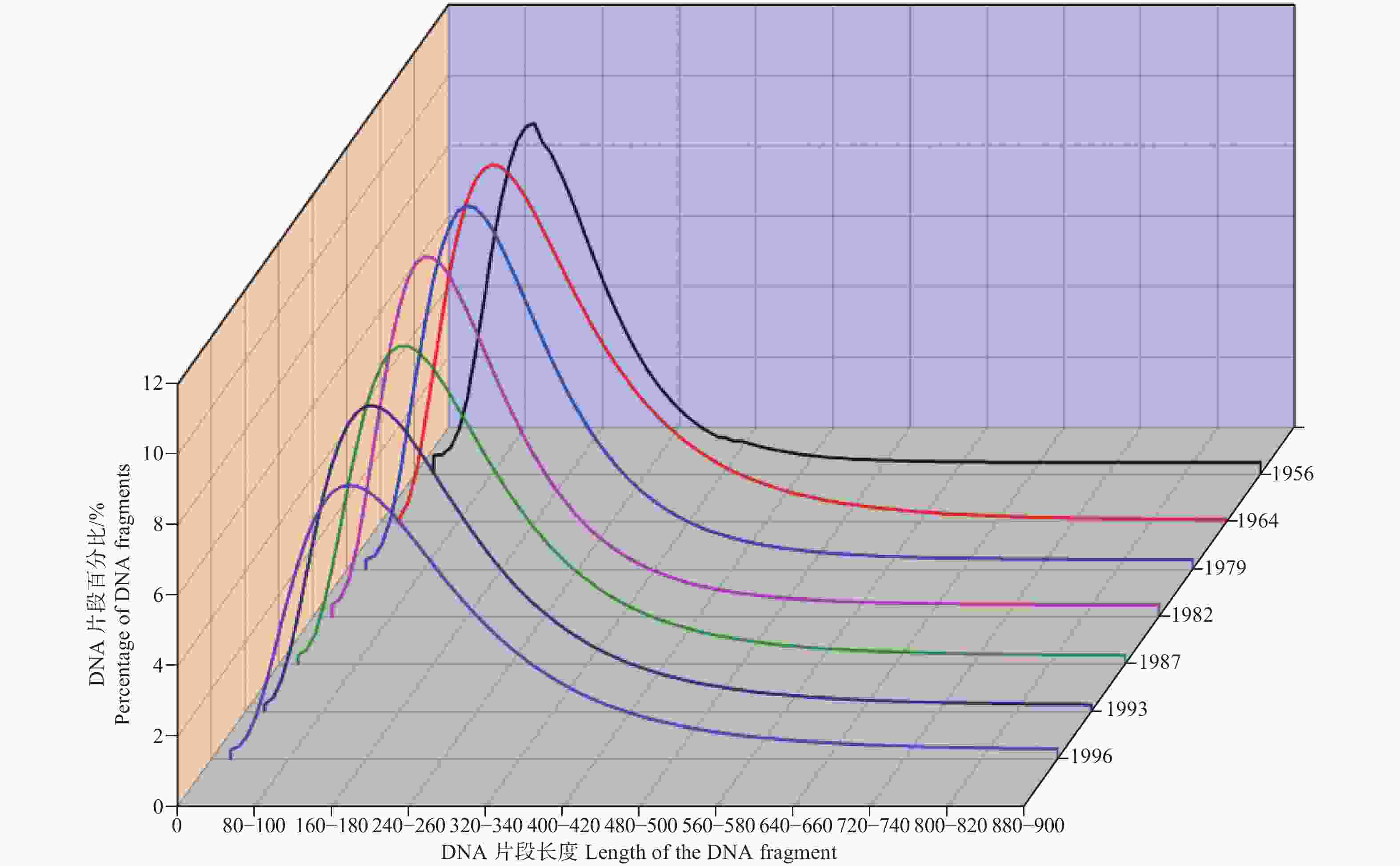
图 3 舞毒蛾标本的DNA片段百分比分布图
Figure 3. The percentage distributions of DNA fragments for L. dispar specimen
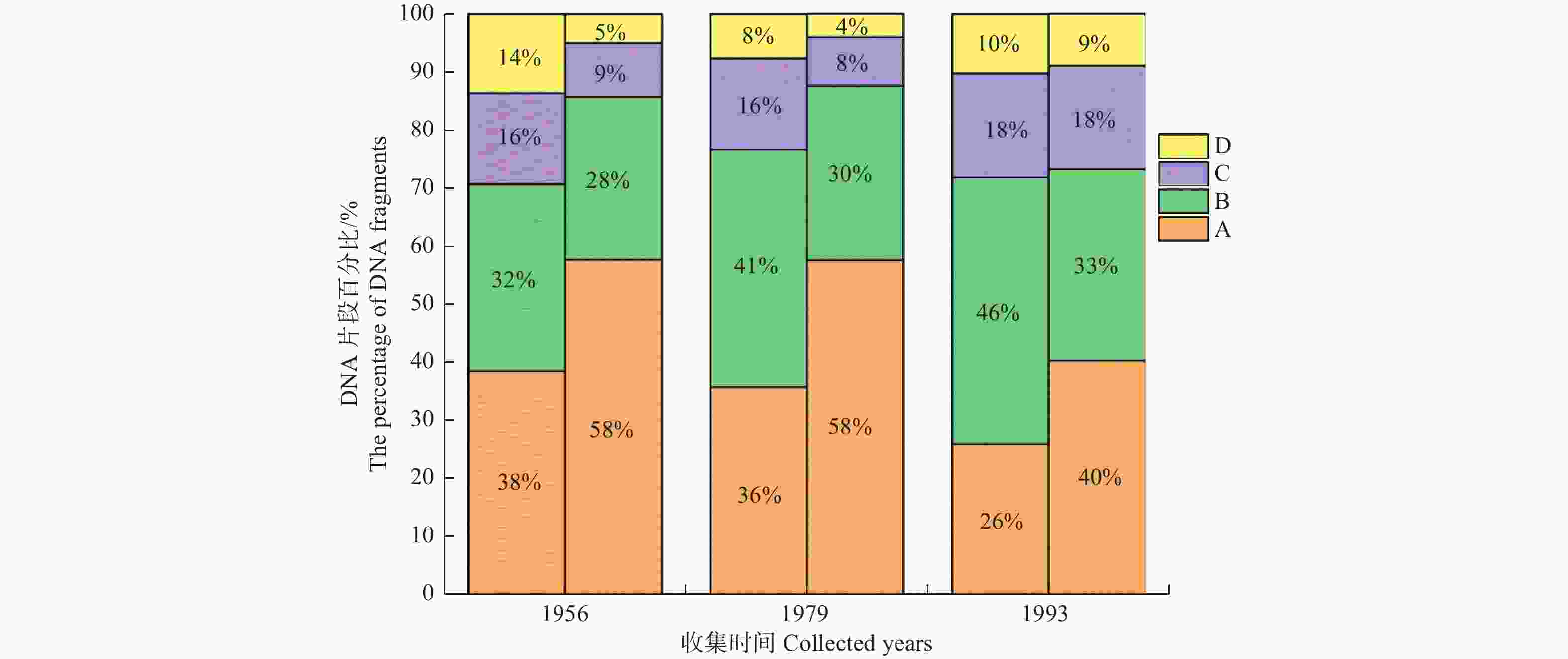
另外,本研究发现对于收集时间相同的福尔马林标本和干燥标本,福尔马林保存的舞毒蛾标本其总体扩增成功率比干燥标本的略高,其中1956年、1979年和1993年收集的福尔马林标本的扩增成功率分别为33.33%、46.67%和73.33%,而干燥标本的扩增成功率分别为26.67%、40.00%和53.33%。在干燥成虫标本和福尔马林幼虫标本的DNA片段百分比的堆积柱状图中(图4),本研究展示出四组DNA片段百分比组成在福尔马林幼虫标本和干燥成虫标本之间存在明显差异。而且干燥成虫标本中的小片段DNA比例明显要高于福尔马林幼虫标本的小片段DNA比例(1-8组DNA片段);相反的,干燥成虫标本中的大片段DNA比例明显低于福尔马林幼虫标本的大片段DNA比例(9-44组DNA片段)。
-
通过比较分析SDS法、磁珠法以及E.Z.N.A.TM昆虫DNA提取试剂盒3种方法对舞毒蛾新鲜样本、干燥标本和福尔马林标本的DNA提取效果,本研究发现E.Z.N.A.TM昆虫DNA提取试剂盒更适合馆藏的舞毒蛾干燥标本和福尔马林标本的DNA提取。SDS法在DNA提取时利用SDS(十二烷基硫酸钠)破坏细胞壁并裂解DNA-蛋白质复合体,使DNA释放出来。但在标本中细胞内的DNA-蛋白质的交联现象加重,使得SDS(十二烷基硫酸钠)无法有效裂解DNA-蛋白质复合体,因此减少了标本中DNA的释放。同时SDS法中常用到的氯仿、苯酚等提取剂也无法完全清除,使得标本DNA提取纯度降低,因此SDS法提取的模板DNA不利于进行PCR扩增等下一步实验。近年来,磁珠法由于其操作过程相对简单、快速,不需要氯仿等有毒溶剂的抽提,也无需过多离心、沉淀等耗时的纯化步骤,而且能够提高DNA提取纯度,在标本DNA提取方面的应用越来越广泛[18, 33]。但是磁珠法DNA提取效果常常受磁珠量的影响。当磁珠量过少时,由于磁珠表面的DNA吸附量有限,因此使得标本DNA未能被完全吸附;当磁珠量过多时,由于磁棒对磁珠的吸附能力有限导致部分磁珠未能被吸附,从而使部分磁珠吸附的DNA被浪费。因此为了达到最好的磁珠法提取效果,试验时应该适当控制磁珠量。E.Z.N.A.TM昆虫DNA提取试剂盒虽然提取过程较磁珠法复杂,同时需要用到氯仿等有毒溶剂的抽提,但其在标本DNA提取过程中用到的裂解、抽提缓冲液以及纯化溶剂能够很好的裂解组织细胞并将DNA释放出来,DNA提取纯度也较高,因此该法利用相对较少的标本材料即能提取到相对较高浓度和纯度的DNA。因此虽然E.Z.N.A.TM昆虫DNA提取试剂盒和磁珠法基因组DNA抽提试剂盒对于舞毒蛾干燥标本和福尔马林标本的提取效果都较SDS法好,但是从节省珍贵标本资源的角度出发,本研究更倾向于利用E.Z.N.A.TM昆虫DNA提取试剂盒进行舞毒蛾干燥标本和福尔马林标本的DNA提取。
本研究发现在标本馆的保存环境下标本保存时间越久扩增长序列目的片段的成功率越低,这可能与标本保存过程中DNA发生降解有关。一方面新鲜活体被做成标本后其体内的代谢活动停止,细胞内的酶系统失去调控而导致体内DNA开始被降解,但在标本保存一段时间后其细胞内的水分会逐渐丢失从而导致体内酶失活,DNA自身降解作用也会逐渐停止。因此标本体内是否保留水分以及保留水分的时间长短对标本DNA的降解至关重要[17]。另一方面我们以前的研究表明(未发表)在标本保存足够时间后(比如保存时间大于18 a),标本馆中的环境如湿度和温度同样会对标本体内DNA降解产生影响,从而导致DNA片段降解程度在保存时间不同的标本中存在差异,标本保存时间越久其体内的DNA降解越严重,提取DNA中的大片段DNA(>400 bp)含量越低,因此扩增大片段目的序列越困难。此外,本研究表明福尔马林幼虫标本的扩增成功率比干燥成虫标本的略高,因此福尔马林幼虫标本的DNA降解程度略低于干燥成虫标本的DNA降解程度。这可能与干燥标本在保存前的处理以及标本馆的环境有关。干燥标本在保存之前未完全干燥,使得标本体内保存水分,细胞内的酶系统继续降解体内DNA;标本馆环境湿度较大或者存在其他影响DNA降解的因素也可能加剧干燥标本体内的DNA降解作用。而对于福尔马林保存的幼虫标本,常因为福尔马林成分中的甲醛被氧化成甲酸而导致DNA降解。但是在用福尔马林保存标本时常会在瓶口部位缠绕封口膜以减少福尔马林与空气的接触,防止甲醛氧化成甲酸从而降低了对标本DNA的损伤。因此,本研究表明干燥成虫标本DNA降解程度比福尔马林幼虫标本的DNA降解程度要严重。但是,本研究及以前研究表明福尔马林标本的DNA提取困难,而且样本中存在很多PCR抑制剂[36],因此本研究不建议利用福尔马林保存标本。另外,福尔马林幼虫标本与干燥成虫标本的DNA降解程度差异也有可能与2种标本的保存虫态有关。
标本中的分子数据是进行物种系统地理学、物种进化研究的重要信息,而标本DNA提取是获得标本分子数据的基础步骤,因此标本DNA提取方法的选择和优化是有效提取标本分子数据的关键。所以在尝试利用标本进行分子生物学研究时,首先需要对DNA提取方法进行讨论分析。本研究表明标本在处理、保存过程中发生了DNA降解,因此在标本收集保存过程中应该尽量避免导致DNA降解的操作。例如,将一部分收集的新鲜样本直接完全干燥不做还软处理即保存于标本馆中,这将降低标本体内的水分以及水分保留时间,从而减少标本DNA自身降解的持续时间,降低标本DNA的降解程度保留更多的长片段基因序列,以便将来可利用这些标本进行分子生物学研究;而另外一部分标本可在完全干燥后展翅保存以便进行形态学研究。标本的保存条件(温度、湿度等)也可能加剧标本体内的DNA降解作用,因此在标本保存过程中应该适当调节标本馆的环境温度和湿度,例如降低标本保存的温度和湿度,最适合标本保存的温度和湿度等还需要进一步研究。以前的研究表明标本的保存方式会对基因序列的扩增成功率产生影响[24, 37-38],闫华超等[24]比较了甲醛、不同浓度乙醇保存标本和自然干燥标本的DNA降解程度,结果表明75%乙醇保存的蜜蜂标本DNA降解程度最低;郑斯竹等[33]也表明无水乙醇−20 ℃保存的天牛标本比干燥标本的PCR扩增成功率高。本研究表明干燥成虫标本的PCR扩增成功率低于福尔马林幼虫标本的PCR扩增成功率,因此为了不影响利用标本进行分子生物学实验并减少采集标本的损失,可在短时间内利用适当浓度的乙醇溶液保存标本。此外,本研究建议在利用标本获取分子数据之前提前检测标本中的DNA片段分布和各片段的百分比分布,这将有利于为引物设计提供直接证据并减少标本资源的损失。
-
本研究表明与SDS法和磁珠法相比,E.Z.N.A.TM昆虫DNA提取试剂盒更适合舞毒蛾新鲜样本、干燥成虫标本和福尔马林幼虫标本的DNA提取,而且提取过程中未对标本DNA产生额外损伤。舞毒蛾标本的保存时间和保存方式均会对基因序列扩增产生影响,标本保存时间越久扩增长序列目的片段的成功率越低,而且福尔马林幼虫标本总体扩增成功率比干燥成虫标本的略高
致谢:本研究感谢中国林业科学研究院森林生物标本馆以及昆虫病毒研究中心提供的舞毒蛾样本。本研究还要感谢中国林业科学研究院森林生态环境与保护研究所张苏芳副研究员在试验过程中给予的帮助和建议。
舞毒蛾标本DNA提取和COI基因扩增
DNA Extraction and COI Gene Amplification of Lymantria dispar Specimens
-
摘要:
目的 探讨适合舞毒蛾标本的保存和DNA提取方法,分析舞毒蛾标本的保存时间和保存方式对基因序列扩增的影响。 方法 利用SDS法、磁珠法以及E.Z.N.A.™昆虫DNA提取试剂盒3种方法对舞毒蛾新鲜样本、干燥成虫标本和福尔马幼虫林标本进行DNA提取,并对3种方法提取DNA的浓度和纯度进行分析比较。利用1956年至1996年收集的舞毒蛾干燥成虫标本和福尔马林幼虫标本分析并比较保存时间和保存方式对15对COI基因(cytochrome oxidase subunit I)引物(目的片段长度为216 bp~977 bp)扩增成功率的影响。 结果 表明与SDS法和磁珠法相比,E.Z.N.A.™昆虫DNA提取试剂盒对舞毒蛾3种标本的DNA提取效果最好,提取过程中未对标本DNA产生额外损伤。标本保存时间越久扩增长序列目的片段的成功率越低,福尔马林幼虫标本总体扩增成功率比干燥成虫标本的略高。 结论 E.Z.N.A.™昆虫DNA提取试剂盒更适合舞毒蛾新鲜样本、干燥成虫标本和福尔马林幼虫标本的DNA提取。舞毒蛾标本的保存时间和保存方式均会对基因序列扩增产生影响。 Abstract:Objective The preservation and DNA extraction methods for Lymantria dispar specimens were discussed, and the effects of storage time and preservation methods of L. dispar specimens on amplification of gene sequences were analyzed. Method Genomic DNA of L. dispar specimens (dried adult, formalin-fixed larval and fresh larval specimens) was extracted by SDS method, the magnetic bead method, and the E.Z.N.A.TM Insect DNA extraction kit. Moreover, the concentration and purity of extracted genomic DNA obtained by the three methods were analyzed and compared. The L. dispar specimens collected from 1956 to 1996 were used to analyze and compared the effects of storage time and preservation methods on the amplification success rate of 15 pairs of COI (cytochrome oxidase subunit I) gene primers (the length of the target fragment is 216 bp to 977 bp). Result The results showed that the concentration and purity of extracted genomic DNA by E.Z.N.A.TMInsect DNA extraction kit was the highest compared with the SDS method and the magnetic bead method. And the specimens' DNA was not damaged during the extraction process. The amplification success rate of specimens with longer storage time was reduced. Moreover, the overall amplification success rate of formalin-fixed larval specimens was slightly higher than that of dried adult specimens. Conclusion The E.Z.N.A. TM Insect DNA extraction kit is more suitable for DNA extraction of L. dispar specimens (dried adult, formalin-fixed larval and fresh larval specimens). The amplification of gene sequences is affected by the storage time and preservation method of L. dispar specimens. -
Key words:
- Lymantria dispar
- / specimens
- / DNA extraction
- / formalin
- / COI gene
-
表 1 本研究所用的舞毒蛾标本
Table 1. Lymantria dispar specimens used in this study
收集地点Collection locality 收集年份Collected year 保存方法Type of preservation 样本数量Number of samples 黑龙江Heilongjiang 1956 干燥成虫dried adult 6 内蒙古Inner Mongolia 1956 福尔马林幼虫formalin larva 5 河北Hebei 1964 干燥成虫dried adult 5 黑龙江Heilongjiang 1979 干燥成虫dried adult 5 辽宁Liaoning 1979 福尔马林幼虫formalin larva 5 北京Beijing 1982 干燥成虫dried adult 5 北京Beijing 1987 干燥成虫dried adult 6 四川Sichuan 1993 干燥成虫dried adult 5 四川Sichuan 1993 福尔马林幼虫formalin larva 10 USA, Newark, DE 1996 干燥成虫dried adult 8 辽宁Liaoning 2018 新鲜幼虫fresh larva 8 注:新鲜样本标注的是提取时间。
Note: the extraction time of fresh samples is recorded.表 2 本研究所用的引物
Table 2. All primers used in this study
引物名称Primers name 引物方向Direction 核苷酸序列5′-3′Nucleotide sequence 5′-3′ 长度Length/bp 退火温度Anneal temperatures/℃ Lco 1 F GCATGAGCTGTAACAATAG 216 49.6 R CAATTTATCGCTTAAACTCAGCC Lco 2 F CCAATTACCAAATCCTCC 274 48.0 R CAATTTATCGCTTAAACTCAGCC Lco 3 F GGATAATCCTTTATGAATGGGG 285 51.0 R CGACGATACTCTGATTACCCAG Lco 4 F CCTGAAAATAGTGGATATCAGTG 303 54.3 R CACGAGCTTACTTTACCTCTGC Lco 5 F GGGGGAAAAGAGCAATTCGTTG 320 52.3 R CGTTCTTTCTATAGGAGCAG Lco 6 F GGGAAATTATTCAAATCCTGG 357 49.6 R GCTCATGGAGGTAGATCTGTTG Lco 7 F CCAGCTAAGTGAAGAGAAA 386 48.0 R ATCAGGAATAGTGGGAAC Lco 8 F TTTTTCCTCTTTCTTGGG 420 48.5 R GGATGAACTGTTTACCCTC Lco 9 F GGGTAATCAGAGTATCGTCG 477 48.5 R TTATTGTTTGGGCTCACCAC Lco 10 F TGGTGAGCCCAAACAATAAA 516 48.5 R AAAATGGAGCAGGAACAGGA Lco 11 F GCAGGGTCAAAAAAGGAT 557 48.5 R TCGAGCTGAATTAGGGAA Lco 12 F TCAGAGAATAGAAGGTGAGT 670 48.5 R TTGTAGAAAATGGAGCAG Lco 13 F CCTAATCTTCAGAGAATAGAAGGTGAGT 766 52.0 R GGAGCCCCTGATATAGCTTTCCCCCG Lco 14 F CCTGAAAATAGTGGATATCAGTG 845 48.5 R TGGAGCAGGAACAGGA Lco 15 F GGGTAATCAGAGTATCGTCG 977 48.5 R AGAAAATGGAGCAGGAACAG 表 3 不同方法提取DNA的浓度与纯度
Table 3. The concentration and purity of genomic DNA extracted by different methods
SDS法
SDS method磁珠法
Magnetic bead method昆虫DNA提取试剂盒
Insect DNA Kit收集时间
Collected yearDNA浓度/
DNA concentration/(ng·μL−1)A260/A280 DNA浓度
DNA concentration/(ng·μL−1)A260/A280 DNA浓度
DNA concentration/(ng·μL−1)A260/A280 干燥成虫
Dried adult1956 124.569 1.592 198.471 2.013 297.778 1.817 福尔马林幼虫
Formalin larval1956 — — 13.172 1.752 15.099 1.823 干燥成虫
Dried adult1979 146.203 1.645 183.012 1.965 298.682 1.795 福尔马林幼虫
Formalin larval1979 12.181 2.276 15.191 1.892 19.164 1.850 干燥成虫
Dried adult1993 143.643 1.541 212.776 1.874 309.136 1.802 福尔马林幼虫
Formalin larval1993 15.704 2.103 22.903 1.896 28.193 1.834 新鲜活体
Fresh sample2018 208.994 1.647 445.383 1.842 451.766 1.853 注:表中数据为每种标本所有样本的DNA浓度与纯度的平均值。
Note: DNA concentration and purity of all samples per specimen are averaged. -
[1] Wandeler P, Hoeck P E A, Keller L F. Back to the future: museum specimens in population genetics[J]. Trends in Ecology and Evolution, 2007, 22(12): 634-642. doi: 10.1016/j.tree.2007.08.017 [2] Yeates D K, Zwick A, Mikheyev A S. Museums are biobanks: unlocking the genetic potential of the three billion specimens in the world's biological collections[J]. Current Opinion in Insect Science, 2016, 18(4): 83-88. [3] DeChaine E G, Martin A P. Historical biogeography of two alpine butterflies in the Rocky Mountains: broad-scale concordance and local-scale discordance[J]. Journal of Biogeography, 2005, 32(11): 1943-1956. doi: 10.1111/j.1365-2699.2005.01356.x [4] Braby M F, Pierce N E, Vila R. Phylogeny and historical biogeography of the subtribe Aporiina (Lepidoptera: Pieridae): implications for the origin of Australian butterflies[J]. Biological Journal of the Linnean Society, 2010, 90(3): 413-440. [5] Stuart B L, Fritz U. Historical DNA from museum type specimens clarifies diversity of Asian leaf turtles (Cyclemys)[J]. Biological Journal of the Linnean Society, 2010, 94(1): 131-141. [6] Mende M B, Hundsdoerfer A K. Mitochondrial lineage sorting in action-historical biogeography of the Hyleseuphorbiae complex (Sphingidae, Lepidoptera) in Italy[J]. BMC Evolutionary Biology, 2013, 13(1): 83-85. doi: 10.1186/1471-2148-13-83 [7] Hernández S, Daley R, Walker T, et al. Demographic history and the south pacific dispersal barrier for school shark (Galeorhinus galeus) inferred by mitochondrial DNA and microsatellite DNA mark[J]. Fisheries Research, 2015, 167: 132-142. doi: 10.1016/j.fishres.2015.02.010 [8] Holmes M W, Hammond T T, Wogan G O, et al. Natural history collections as windows on evolutionary processes[J]. Molecular Ecology, 2016, 25(4): 864-881. doi: 10.1111/mec.13529 [9] Xu Y, Zhang S, Wang H, et al. Mitochondrial gene sequence (COI) reveals the genetic structure and demographic history of Lymantriadispar (Lepidoptera: Erebidae: Lymantriinae) in and around China[J]. Insects, 2019, 10(5): 146-165. doi: 10.3390/insects10050146 [10] Krehenwinkel H, Pekar S. An analysis of factors affecting genotyping success from museum specimens reveals an increase of genetic and morphological variation during a historical range expansion of a European Spider[J]. PLoS ONE, 2015, 10(8): e0136337. doi: 10.1371/journal.pone.0136337 [11] Mikheyev A S, Tin M M, Arora J, et al. Museum samples reveal rapid evolution by wild honey bees exposed to a novel parasite[J]. Nature Communications, 2015, 6(1): 7991. doi: 10.1038/ncomms8991 [12] Strutzenberger P, Brehm G, Fiedler K. DNA barcode sequencing from old type specimens as a tool in taxonomy: a case study in the diverse genus Eois(Lepidoptera: Geometridae)[J]. PLoS ONE, 2012, 7(11): e49710. doi: 10.1371/journal.pone.0049710 [13] Price B W, Henry C S, Hall A C, et al. Singing from the grave: DNA from a 180 year old type specimen confirms the identity of Chrysoperla carnea (Stephens)[J]. PLoS ONE, 2015, 10(4): e0121127. doi: 10.1371/journal.pone.0121127 [14] Strange J P, Knoblett J, Griswold T. DNA amplification from pin-mounted bumble bees (Bombus) in a museum collection: effects of fragment size and specimen age on successful PCR[J]. Apidologie, 2009, 40(2): 134-139. doi: 10.1051/apido/2008070 [15] Miller J A, Beentjes K K, Helsdingen P, et al. Which specimens from a museum collection will yield DNA barcodes? A time series study of spiders in alcohol[J]. ZooKeys, 2013, 365: 245-261. doi: 10.3897/zookeys.365.5787 [16] Gilbert M T P, Moore W, Melchior L, et al. DNA extraction from dry museum beetles without conferring external morphological damage[J]. PLoS ONE, 2007, 2(3): e272. doi: 10.1371/journal.pone.0000272 [17] 胡泽章, 黄 建, 王竹红. 昆虫标本DNA提取的研究进展[J]. 武夷科学, 2013, 29(1):165-170. doi: 10.3969/j.issn.1001-4276.2013.01.022 [18] 李枷霖, 郑斯竹, 蔡 平, 等. 不同预处理方法影响昆虫干标本DNA提取效果[J]. 基因组学与应用生物学, 2015, 34(2):396-402. [19] Guzman-Larralde A J, Suaste-Dzul A, Adrien G, et al. DNA recovery from microhymenoptera using six non-destructive methodologies with considerations for subsequent preparation of museum slides[J]. Genome, 2017, 60(1): 85-91. doi: 10.1139/gen-2015-0172 [20] 魏亦寒, 郑斯竹, 蔡 平, 等. 粉蚧标本保存与DNA提取方法的比较[J]. 应用昆虫学报, 2015, 52(4):925-932. doi: 10.7679/j.issn.2095-1353.2015.111 [21] Hunter S J, Goodall T I, Walsh K A, et al. Nondestructive DNA extraction from blackflies (Diptera: Simuliidae): retaining voucher specimens for DNA barcoding projects[J]. Molecular Ecology Resources, 2008, 8(1): 56-61. doi: 10.1111/j.1471-8286.2007.01879.x [22] 徐来祥, 张知彬, 宋铭晶, 等. 福尔马林保存的动物标本基因组DNA的提取方法[J]. 动物学报, 2002, 48(2):264-269. doi: 10.3321/j.issn:0001-7302.2002.02.017 [23] 张晟铭, 张 真, 王鸿斌, 等. 不同保存条件下云杉八齿小蠹总DNA提取方法的比较分析[J]. 安徽农业科学, 2009, 37(13):5883-5885. doi: 10.3969/j.issn.0517-6611.2009.13.027 [24] 闫华超, 贾少波, 王雪梅. 不同方法保存的蜜蜂基因组DNA提取的比较[J]. 生物技术通讯, 2011, 22(5):726-728. doi: 10.3969/j.issn.1009-0002.2011.05.029 [25] 魏方超, 杨茂发, 彭 瑶, 等. 稻水象甲AFLP分析中基因组DNA提取方法的研究[J]. 贵州农业科学, 2012, 40(9):129-132. doi: 10.3969/j.issn.1001-3601.2012.09.035 [26] 赵 清, 张佳庆, 张虎芳. 蝽类昆虫干制标本基因组提取及相关基因扩增[J]. 山西农业大学学报: 自然科学版, 2015, 35(5):478-483. [27] 湛孝东, 李朝品, 席贻龙. 几种单头螨线粒体基因组提取方法的比较[J]. 中国医学创新, 2015, 12(18):1-4. doi: 10.3969/j.issn.1674-4985.2015.18.001 [28] Bisanti M, Ganassi S, Mandrioli M. Comparative analysis of various fixative solutions on insect preservation for molecular studies[J]. Entomologia Experimentalis Et Applicata, 2010, 130(3): 290-296. [29] Zimmermann J, Hajibabaei M, Blackburn D C, et al. DNA damage in preserved specimens and tissue samples[J]. Frontiers in Zoology, 2008, 5(1): 1-13. doi: 10.1186/1742-9994-5-1 [30] Sutrisno H. The impact of storage times of museum insect specimens on PCR success: case study on moth collections in Indonesia[J]. HAYATI Journal of Biosciences, 2012, 19(2): 99-104. doi: 10.4308/hjb.19.2.99 [31] 季清娥, 杨建全, 吕宝乾, 等. 不同保存条件下茧蜂标本基因组DNA的降解[J]. 华东昆虫学报, 2005, 14(2):15-17. [32] 曲良建, 王丽娟, 王青华, 等. 松墨天牛成虫标本保存及其DNA提取质量比较[J]. 应用昆虫学报, 2014, 51(3):741-748. doi: 10.7679/j.issn.2095-1353.2014.089 [33] 郑斯竹, 安榆林, 徐 梅, 等. 多年保存天牛科标本的DNA微量提取方法[J]. 植物检疫, 2012, 26(3):30-34. [34] 孔啸兰, 陈作志, 林 琳, 等. 福尔马林固定鱼类标本DNA提取方法的优化[J]. 中国水产科学, 2012, 19(5):1068-1073. [35] 蒋欣悦. 毒死蜱降解菌的分离、鉴定以及联合植物促生菌对土壤的改良[D]. 上海: 上海师范大学. 2015, 32-33. [36] 夏颖哲, 盛 岩, 陈宜瑜. 福尔马林对固定标本DNA提取和扩增的影响[J]. 四川动物, 2006, 25(3):662-665. doi: 10.3969/j.issn.1000-7083.2006.03.063 [37] 张迎春, 刘 波, 郑哲民, 等. 不同保藏处理的昆虫标本DNA提取及其随机扩增多态DNA反应[J]. 昆虫学报, 2002, 45(5):693-695. doi: 10.3321/j.issn:0454-6296.2002.05.026 [38] 闫 晗, 董 君, 黄 静, 等. 不同固定剂处理的对虾基因组DNA提取方法研究[J]. 应用化工, 2012, 41(3):548-551. doi: 10.3969/j.issn.1671-3206.2012.03.054 -




 下载:
下载: