-
目前国内关于凋落物对土壤酶活性影响的研究,主要以改变凋落物种类或者改变凋落物组成为主[1-3],而以不同林龄序列为研究对象,通过改变地表凋落物输入量,进而改变有机质输入量,研究碳源输入对土壤酶活性影响的实验较少,尤其是在亚热带—温带气候过渡区。除此之外,森林生态系统土壤C的积累是一个缓慢而且复杂的过程[4],到目前为止,改变地表凋落物输入量对土壤C含量的影响还没有达成共识[5],并且已有实验研究表明碳输入量的改变能够影响土壤微生物量、微生物群落结构以及微生物活性[6]。目前许多生态学家主要采用DIRT实验和室内控制实验从而改变碳输入量,以探究不同数量和质量的植物体有机C输入对土壤养分、微生物群落结构以及土壤C循环过程的影响[7-8]。作者以不同年龄序列(林龄大约为40年、80年和大于160年)的天然锐齿栎林为研究对象,通过人为改变锐齿栎林林下土壤碳输入量,对土壤酚氧化酶、过氧化物酶、β-葡萄糖苷酶和N-乙酰-β葡萄糖苷酶的活性以及土壤理化性质、微生物生物量进行测定分析,旨在探讨土壤酶活性与碳输入量之间的关系,为揭示森林土壤养分碳循环以及土壤碳的管理提供基本理论支持。
HTML
-
本研究区处于北亚热带气候向南暖温带气候过渡区的河南宝天曼自然保护区长期森林生态定位站(33°20′~33°36′ N,111°46~112°04′ E,海拔600~1 830 m)。气候类型属于季风型大陆性气候,年均温15.1℃,年均降雨量900 mm,年蒸发量991.6 mm,相对湿度68%,极端最高温41.2℃,极端最低温-14.8℃,≥10℃的年积温4 200~4 900℃,无霜期高山区160 d,低山区227 d。土壤类型主要以风化的砂质岩演化而成的不饱和始成土为主,植被类型属于北亚热带常绿阔叶林向南暖温带落叶林过渡的典型代表,以栎类植物为优势树种[9-10]。
-
选取3个龄级的锐齿栎林作为研究对象,分别为:幼龄林(约40 a),中龄林(约80 a),和老龄林(约160 a), 林龄由森林经营记录结合平均木生长锥获得。每组年龄随机布设3块20 m×20 m的样地。于2011年6月在每块样地中采用随机区组设计,布设9个2 m×2 m小样方,分为3个区组,每个区组内分别进行对照(CK)、去除(去凋凋落物,LR)和加倍(加倍凋落物,LA)处理。把实验小样方中的地表凋落物全部移除作为去除地表凋落物处理,把去除凋落物处理小样方中的凋落物全部均匀加入到相应的小样方中作为加倍凋落物处理,以未经过任何处理的作为自然对照(CK),并在试验过程中定期进行样地维护。
于2015年8月,用内径5 cm的土钻“S”型采集地表 0~5 cm土壤样品,混匀后挑拣出石砾和根系等杂物后过2 mm筛后混匀并分成2份,一份用于测定土壤基本理化性质,另一份保存于-20℃用于测定土壤酶活性。
-
土壤酶活性的测定采用底物诱导法,测定步骤参照You等[9]的方法:酚氧化酶活性由土壤悬浮液(1 g鲜土+1.5 mL醋酸钠缓冲液)和2 mL L-DOPA混合充分反应后测定(20℃,100 rpm震荡1 h);过氧化物酶活性由土壤悬浮液(1 g鲜土+1.5 mL醋酸钠缓冲液)和2 mL L-DOPA(5 mmol·L-1)充分混合(20℃,100 rpm震荡1 h),再加入0.2 mL H2O2(0.3%)反应后测定。β-葡萄糖苷酶活性和N-乙酰-β-葡萄糖苷酶活性由4 g鲜土和10 mL醋酸钠缓冲液充分混合(100 rpm震荡0.5 h)后,分别加入0.2 mL PNG(50 mmol·L-1)和0.2 mL NAG(10 mmol·L-1),37℃培养1 h后加入氯化钙和Tris缓冲液终止反应后测定。酶活性测定均利用紫外可见分光光度计进行比色,具体基质和培养条件如表 1所示。
酶
Enzyme基质
Substrate培养温度/℃
Incubation temperature培养时间/h
Incubation time测定产物
Determination product酚氧化酶Polyphenol oxidase 左旋多巴胺L-DOPA 20 1 DOPA转化 过氧化物酶Peroxidase 左旋多巴胺+过氧化氢L-DOPA+H2O2 20 1 DOPA转化 β-葡萄糖苷酶β-1, 4-glucosidase 对硝基苯-β-D葡糖苷4-MUB-β-D-glucoside 37 1 对硝基酚 N-乙酰-β-葡萄糖苷酶β-1, 4-N-acetylglucosaminidase 对硝基苯-N-乙酰-β-D-氨基葡糖苷4-MUB-N-acetyl-β-D-glucosaminide 37 1 对硝基酚 Table 1. Substrates, incubation conditions and determination products of soil enzyme activity assays
所有总土壤酶活性单位为μmol·g-1·h-1;专一酶活性采用每单位微生物量C(MBC)的酶活性表示,数值=总土壤酶活性/MBC[11]。
参照Jin等[12]描述的方法,采用室内培养碱式吸收法测定CO2的释放量,计算得到土壤微生物呼吸(Soil microbial respiration, MR):将相当于20 g干土的新鲜土壤放入250 mL的培养瓶中,用10 mL的NaOH(0.1 mol·L-1)溶液吸收培养土壤释放的CO2气体。所有的培养瓶用橡胶瓶盖密封,在黑暗条件25℃中进行恒温连续培养12天,每隔2天用0.05 mol·L-1 HCl滴定NaOH溶液吸收的CO2量;氯仿熏蒸浸提法测定土壤微生物生物量C(MBC)和微生物生物量N(MBN):称取5 g新鲜土壤于培养瓶中在黑暗恒温条件下进行氯仿熏蒸24 h,用20 mL 0.5 mol·L-1 K2SO4溶液进行浸提(20℃,100 r·min-1震荡0.5 h),浸提液利用总有机碳分析仪(TOC)进行测定;重铬酸钾氧化-外加热法测定土壤有机碳;利用pH计(STARTER2100,OHAUS)对土壤pH进行测定:水土比2.5:1充分混合后(20℃,100 r·min-1震荡0.5 h)测定;烘干法测定土壤质量含水量:称取15 g鲜土于铝盒中,在105±2℃条件下烘干土壤至恒质量(至少48 h)后通过计算得到。
利用统计软件SPSS19.0对数据进行统计和方差分析(ANOVA),多重比较不同处理间的差异性(P < 0.05);在多元统计分析软件Canoco for Windows 4.5上进行主成分分析,分析凋落物处理对土壤专一酶活性变异程度的影响;在软件Sigma Plot 12.0上完成作图。
1.1. 研究区概况
1.2. 实验设计与采样
1.3. 样品测定和数据处理
-
如表 2、表 3所示,3组不同龄级的锐齿栎之间,仅土壤pH和微生物呼吸受林龄的影响,均在中龄林中最高,老龄林次之,幼龄林最低。改变碳输入方式对幼龄林和中龄林的土壤微环境和微生物生物量碳氮无影响。老龄林中,碳输入方式的改变对土壤pH和微生物生物量碳氮比产生一定影响,与对照组相比,去除凋落物处理显著增加土壤pH值,加倍凋落物处理显著降低微生物的碳氮比(P < 0.05)。
林龄
Age/a处理
Treatment%SWC
/(w/w)pH
/(2.5:1)SOC
/(g·kg-1)MBC
/(mg·kg-1)MBN
/(mg·kg-1)C/Nmic MR
/(mg·g-1·d-1)幼龄
40对照CK 33.6±0.3a 4.5±0.0a 56.4±2.4a 495.3±27.0a 45.4±3.1a 10.2±0.3a 0.62±0.01a 加倍LA 33.7±0.7a 4.5±0.0a 52.0±7.8a 762.8±66.0a 77.0±9.2a 10.1±0.4a 0.59±0.02a 去凋LR 32.7±0.8a 4.4±0.0a 48.7±4.3a 446.7±8.7a 36.0±1.9a 12.6±0.6a 0.57±0.01a 中龄
80对照CK 32.9±3.0a 4.9±0.0a 37.6±3.2a 338.8±61.0a 51.5±3.7a 11.4±0.9a 0.65±0.02a 加倍LA 28.2±3.5a 4.8±0.0a 63.2±3.8a 475.3±36.0a 46.6±1.5a 11.1±1.0a 0.68±0.02a 去凋LR 34.7±1.7a 4.9±0.0a 49.7±0.9a 167.0±59.2a 32.0±0.6a 5.3±1.4a 0.70±0.01a 老龄
160对照CK 33.3±1.7a 4.6±0.0b 61.9±1.6a 375.5±53.8a 28.1±3.9a 12.8±0.4a 0.67±0.01a 加倍LA 36.8±2.1a 4.6±0.0b 60.2±3.5a 487.3±34.0a 47.6±3.3a 7.4±1.0b 0.68±0.02a 去凋LR 31.9±1.2a 4.7±0.0a 48.0±6.3a 515.8±65.1a 49.2±7.7a 10.6±0.2ab 0.64±0.02a 注:同列不同小写字母表示处理间差异性显著。%SWC:土壤质量含水量;SOC:土壤有机碳含量;MBC:微生物生物量碳;MBN:微生物生物量氮;C/Nmic:微生物碳氮比;MR:微生物呼吸。
Note: Different letters in the same column indicate significant effect (at P=0.05 level).%SWC: gravimetric soil water content (w/w); pH: soil pH value; SOC: soil organic carbon concentration; MBC: microbial biomass carbon; MBN: microbial biomass nitrogen; C/Nmic; microbial C/N; MR: microbial respiration.Table 2. Soil chemical and physical properties and microbial community characteristics (mean±std. error)
因素 自由度 %SWC pH SOC MBC MBN C/Nmic MR 林龄 2 1.447 56.91*** 1.002 2.226 1.049 1.078 26.137*** 处理 2 0.223 0.947 1.863 1.498 1.432 0.642 0.399 林龄×处理 4 0.280 1.622 0.728 2.498 1.763 0.695 3.350** 注:**P < 0.01, ***P < 0.001.
Note: **and *** Denote significant correlations at P < 0.01 and P < 0.001, respectively.Table 3. Summary of F-values and significance level in ANOVA evaluating the effects of stand age and treatment on soil chemical and physical properties and microbial community characteristics
-
研究结果表明,N-乙酰-β葡萄糖苷酶活性受林分年龄的影响显著(P < 0.05),而其他3种酶活性受林分年龄的影响不显著(P>0.05),2种水解酶(β-葡萄糖苷酶、N-乙酰-β葡萄糖苷酶)受碳输入方式的影响显著(P < 0.05)(表 4)。
因素 自由度 酚氧
化酶过氧
化物酶β-葡萄
糖苷酶N-乙酰-β
葡萄糖苷酶林龄 2 0.919 0.658 0.154 3.577* 处理 2 0.786 0.255 9.099** 3.888* 林龄×处理 4 0.202 0.202 2.526 0.456 注:*P < 0.05;**P < 0.01.
Note: * and ** Denote significant correlations at P < 0.05 and P < 0.01, respectively.Table 4. Summary of F-values and significance level in ANOVA evaluating the effects of stand age and treatment on soil total enzyme activities.
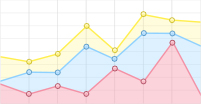
如图 1A和图 1B所示,不同处理对土壤氧化酶活性无明显影响,3种林龄中不同处理间氧化酶活性均无显著差异(P>0.05)。在幼龄林和老龄林中不同处理间酚氧化酶活性均为:去凋>对照>加倍,而在中龄林中则表现为:对照>加倍>去凋,3种林龄中酚氧化酶活性总的趋势均为对照高于加倍;3种林龄的不同处理间过氧化物酶活性均表现为:对照>加倍>去凋,其中在幼龄林中加倍处理和去凋处理分别比对照降低了11.6%、45.6%,在中龄林中分别降低了4.3%、10.1%,在老龄林中分别降低了0.8%、28.6%。
如图 1C和图 1D所示,β-葡萄糖苷酶活性在中龄林的不同处理间无显著差异(P>0.05)。幼龄林和老龄林均表现为去凋处理时β-葡萄糖苷酶活性最低,与对照组相比分别降低了29.7%和56.7%;老龄林中加倍处理酶活性增加了29.2%。中龄林和老龄林中不同处理间β-葡萄糖苷酶活性大小表现为:加倍>对照>去凋。幼龄林和中龄林不同处理间N-乙酰-β葡萄糖苷酶活性差异不显著,大小均表现为:对照>加倍>去凋;老龄林与对照相比,加倍处理使N-乙酰-β葡萄糖苷酶活性增加了19.5%,但无显著差异(P>0.05),去凋处理使N-乙酰-β葡萄糖苷酶活性降低了58.6%,差异性显著(P < 0.05)。老龄林中水解酶活性表现为:加倍>对照>去凋。
对3组不同年龄的锐齿栎林土壤专一酶活性(表征微生物功能)进行主成分分析,结果表明,在40 a和80 a的锐齿栎林中,第一主成分轴能把去除凋落物处理与对照和加倍凋落物处理区分开,表明在处理4 a后,去除凋落物处理土壤专一酶活性与对照组和加倍凋落物处理的专一酶活性之间存在明显差异,但加倍凋落物处理与对照组无差异(图 2A和图 2B);在160 a的锐齿栎林中,第一主成分轴能把加倍凋落物处理与对照和去除凋落物处理区分开,而第二主成分轴能把去除凋落物处理与对照组区分开(图 2C),表明在处理4 a后,不管是加倍凋落物还是去除凋落物,都能在一定程度上改变土壤专一酶活性,加倍凋落物处理的效果更明显。
2.1. 改变碳输入对土壤理化性质及微生物性状的影响
2.2. 改变碳输入对土壤酶活性的影响
-
凋落物分解为森林土壤提供大量氮、磷、钾等生长必需的营养元素以及生物量有机碳、氮等[13],去除森林凋落物可以减少土壤养分输入,降低土壤保水能力,加快土壤营养流失,土壤中碳氮含量下降[14],导致土壤微生物的生长受到严重抑制。据相关实验研究发现土壤微生物与土壤有机质呈正相关关系,即土壤有机质含量下降,土壤微生物量和土壤微生物活性也随之降低[15]。虽然土壤对pH值的变化有一定的缓冲能力[16],但在本实验中,3组不同年龄林分长期改变碳源输入对土壤pH及微生物呼吸产生了影响。在幼龄林和老龄林中去除凋落物处理显著降低了土壤有机碳含量,加倍凋落物处理增加了土壤有机碳含量。老龄林中,碳输入方式的改变对土壤pH和微生物生物量碳氮比产生一定影响,与对照组相比,去除凋落物处理显著增加土壤pH值,加倍凋落物处理显著降低微生物的碳氮比。Weintraub等[17]通过实验证明,凋落物是影响土壤有机碳的主要因素,增加凋落物量可显著提高土壤有机碳含量;反之,降低。
-
土壤有机质作为土壤微生物的主要碳源,通过植物凋落物、根系和根系分泌物等形式输入,为酶促反应提供重要底物。改变凋落物输入量不仅直接影响土壤微生物量,还可以改变酶促反应所需底物浓度,进而对土壤酶产生影响。通过分析发现,改变碳源输入对土壤pH产生一定影响,土壤酶活性与土壤pH呈负相关关系(表 5),同时也有相关文献研究表明土壤pH显著影响土壤酶活性[18]。这可能是由于酶空间构象和氨基酸残基微环境易受土壤pH的变化而改变,从而对酶活性产生影响[19],也可能是由于pH的改变造成酶与土壤颗粒之间的结合状态发生改变,导致土壤酶活性发生变化。
变量 %SWC pH值 SOC MBC MBN MR 酚氧化酶Polyhenol oxidase -0.210 -0.080 -0.206 -0.123 -0.057 -0.300 过氧化物酶Peroxidase 0.360 -0.087 0.549* 0.280 0.247 -0.054 β-葡萄糖苷酶β-1, 4-glucosidase 0.314 -0.176 0.510* 0.059 0.055 0.076 N-乙酰-β葡萄糖苷酶β-1, 4-N-acetylglucosaminidase -0.128 -0.391* 0.279 0.364 -0.134 -0.164 注:*P < 0.05。
Note: * Denote significant correlations at P < 0.05, respectivelyTable 5. Pearson's correlations between soil chemical and physical properties, microbial community characteristics and soil total enzyme activities
本实验中,去除凋落物处理中的氧化物酶活性、β-葡萄糖苷酶活性和N-乙酰-β葡萄糖苷酶活性均有不同程度的降低,而这些酶在土壤获取碳、氮等营养元素过程中起到了重要作用,这说明去除凋落物处理造成土壤水解酶生物活性下降,与刘星等[1]在太岳山油松林进行的研究结果一致。杨敬天等[20]通过通径分析研究发现,土壤有机质含量显著影响多种土壤酶生物活性,并且具有显著相关性。碳输入的减少对过氧化物酶和酚氧化酶的影响不显著,可能是因为去除凋落物处理只是减少了土壤地表凋落物的碳输入,而忽略了植物根系也是作为植物碳输入的主要来源。当土壤碳输入减少时,β-葡萄糖苷酶活性和N-乙酰-β-葡萄糖苷酶活性均降低,该结果也从侧面证实了水解酶活性与土壤有机碳含量呈正相关关系,去除凋落物处理切断了凋落物的碳源、氮源输入,减少了土壤中的碳、氮含量,导致β-葡萄糖苷酶和N-乙酰-β-葡萄糖苷酶活性下降。Hernandez等[21]通过相关研究发现,水解酶活性随着相应底物、产物浓度的增加而升高。斯贵才等[22]通过研究也发现水解酶活性与土壤有机碳含量呈显著正相关关系。
不同林分年龄间碳输入减少对酚氧化酶和过氧化物酶活性影响并不显著,在幼龄林和老林龄中经过去除凋落物处理的酚氧化酶活性略有升高,这可能是与植物根系提供大量底物有关。同时,在老龄林中改变碳源输入,β-葡萄糖苷酶活性和N-乙酰-β-葡萄糖苷酶活性均有显著的升高或降低,而在幼龄林和中龄林中无显著变化。这可能是由于不同年龄林分中凋落物成分和微生物群落结构具有差异性:随着林龄的增加,自疏作用越来越明显导致郁闭度降低,光照条件良好使得林内光照更加充足,为土壤微生物的生长和繁殖提供了有利条件,土壤微生物的多样性随土壤微生物数量和种类的增多而增大[23],从幼龄林、中龄林到成熟林随着林分密度及郁闭度先升高后下降的趋势,微生物多样性呈现出“高-低-高”的规律性变化,从而影响土壤微生物活性的变化程度[24]。
-
有关研究结果表明细菌的碳氮比(C/N)通常在3~5之间,而真菌的C/N通常在4~15之间,微生物群落中细菌和真菌的构成情况可以通过当时土壤微生物的C/N反映,土壤微生物C/N越低,在整个土壤微生物群落中细菌群落所占的比重就越大[25]。C输入方式不仅可以通过控制输入C的数量和质量改变土壤微生物群落结构,还可以改变土壤C和N的有效性以及微环境来影响土壤MBC和MBN[26-27]。本研究结果表明,除了在老年林中的加倍凋落物处理中能显著降低土壤微生物C/N,其他林分各个处理之间的微生物C/N均无明显差异,这与Nadelhoffer等[28]在美国马萨诸塞州的落叶林中通过加倍凋落物处理后,发现土壤矿质层细菌或真菌的生物量不随地表凋落物数量的增加而发生改变的研究结论相似。同时,Cusack等研究发现,微生物群落的功能(土壤酶专一酶活性)随着其结构的改变而显著变化[29]。
虽然在40 a和80 a锐齿栎林去除凋落物后,其中微生物C/N无差异,但其专一酶活性却发生明显改变。该结果表明,只通过较短期的观测不能完全区分微生物群落结构和功能之间的关系,原因可能有如下几点:(1)本研究只是通过测定微生物的C/N来表征微生物的结构,这种方法只能粗略反映土壤细菌和真菌的比例,不能精确反映土壤微生物的群落组成;(2)本研究中测定的微生物类群为土壤中所有具有活性的类群,没有考虑微生物实际是否具有活性,实际上土壤中可能有很多微生物处于休眠状态,此类微生物不具有活性。因此,更好的量化微生物群落组成与其生态系统功能之间的关系,需要深入了解微生物功能的冗余[30];(3)环境因素如温度、水分和土壤养分的变化极易引起微生物群落结构和功能的改变[9],但目前由于技术手段原因,还没有一种测量方法可以准确地反映出原状土壤的酶活性[31]。
3.1. 不同处理对土壤理化性质及微生物性状的影响
3.2. 改变碳源输入对土壤酶活性的影响
3.3. 不同碳源输入对土壤微生物群落结构和功能(专一酶活性)的影响
-
(1) 改变碳源输入对幼龄林和中龄林的土壤微环境和微生物生物量碳氮无显著影响,对老龄林的土壤pH和微生物生物量碳氮比产生一定影响。不同龄级的锐齿栎之间,仅土壤pH和微生物呼吸受林龄的影响。
(2) 改变碳源输入对β-葡萄糖苷酶和N-乙酰-β葡萄糖苷酶的活性影响显著;林分年龄对N-乙酰-β葡萄糖苷酶活的影响显著,对其他3种酶影响不显著。除碳输入方式的改变,林分年龄也是影响土壤酶活性的一个重要指标。
(3) 在40 a和80 a的锐齿栎林中,去除凋落物处理土壤专一酶活性与对照组和加倍凋落物处理的专一酶活性之间存在明显差异;在160年的锐齿栎林中,改变碳源输入在一定程度上改变土壤专一酶活性,加倍凋落物处理的效果更明显。但在本研究中,土壤微生物结构(微生物C/N)和功能(专一酶活性)没有必然联系,还需开展更加长期的连续观测,为准确评估特定微生物群落结构与功能之间的关系提供理论依据。







 DownLoad:
DownLoad:
