-
羟自由基作用于体内蛋白质、核酸、脂类等生物分子,造成细胞结构和功能受损,进而导致代谢紊乱引起疾病[1-2]。羟自由基清除能力是评价抗氧化能力的重要指标之一,在抗氧化类保健品和药品研究中得到广泛应用[3-5]。研究人员在梨( Pyrus L.)、软枣猕猴桃( Actinidia arguta Planch. ex Miq.)、石榴( Punica granatum Linn.)、李( Prunus saliceina Linn.)、杏( Armeniaca vulgaris Lam.)、芒果( Mangifera indica Linn.)、柑橘( Citrus reticulate Blanco.)、黑桑( Morus nigra Linn.)、刺山柑( Capparis spinosa L.)等多种植物研究中发现其果实的羟自由基清除能力与酚类物质含量具有显著相关性[6-14]。沙棘( Hippophae rhamnoides L.)属于胡颓子科沙棘属植物,是一种药食同源植物,含有丰富的生物活性物质,其中酚类物质含量尤其丰富[15-18]。目前,对沙棘果实酚类物质的研究主要集中在酚类物质的提取,酚类物质的测定,酚类提取物的作用以及沙棘产品的加工[4, 19-25];而关于不同酚类物质含量与羟自由基清除能力相关性的研究在沙棘果实中研究较少,主要集中在梨、猕猴桃、柑橘等树种[6-7, 12]。因此,本研究以沙棘品种丰宁和向阳不同发育时期果实为研究材料,对沙棘果实提取物的羟自由基清除能力与酚类物质含量间的相关性进行探索,将为评估沙棘果实质量提供参考,同时对于沙棘产品生产加工及沙棘栽培育种过程中的品种选择具有重要意义。
HTML
-
研究材料采自内蒙古磴口县(107°05′ E,40°13′N)的中国沙棘( H.rhamnoides subsp. sinensis )品种丰宁和蒙古沙棘( H.rhamnoides subsp. mongolia )品种向阳的果实。沙棘栽植于沙壤土,处于自然条件下,树龄为12 a。每个品种3个生物学重复,从每棵树的不同部位,东西南北4个方向随机分别摘取3个不同发育时期(分别为绿果期、变色期和成熟期)的果实。所用的标准品维生素E(10191-41-0)、芦丁(153-18-4)、槲皮素(117-39-5)、柚皮素(480-41-1)、杨梅素(529-44-2)、山奈酚(520-18-3)、异鼠李素(480-19-3)购买于百灵威公司。
-
混标工作液配制:量取0.5 mL芦丁(1 mg·mL-1)和0.5 mL异鼠李素(50 μg·mL-1)溶于1.0 mL甲醇配制2.0 mL混标溶液A;量取0.2 mL山萘酚(10 μg·mL-1)、0.2 mL杨梅素(50 μg·mL-1)、0.2 mL柚皮素(50 μg·mL-1)、0.2 mL槲皮素(100 μg·mL-1)和0.2 mL维生素E(500 μg·mL-1)溶于1.0 mL甲醇配制2.0 mL混标溶液B。
衍生化处理:将混标溶液装入衍生化小瓶中,2个平行,放入快速离心干燥仪中挥干。挥干后的标品中加入80.0 μL的甲氧胺盐酸吡啶溶液(15 mg·mL-1),涡旋震荡2 min后,于震荡培养箱中37℃肟化反应90 min,取出后再加入80.0 μL的BSTFA(含1%TMCS)衍生试剂,涡旋震荡2 min后,于70℃反应60 min。取出样本,室温放置30 min[26-28]。
气相质谱-色谱(GC-MS)分析:本实验的分析仪器为Agilent公司的7890A-5975C气相色谱飞行时间质谱联用仪(Agilent,USA),1.0 μL衍生化后的提取物用无分流模式注入GC-MS系统进行分析,样品经非极性的DB-5MS毛细管柱(30 m × 250 μm I.D., J&W Scientific, Folsom, CA)分离后进入质谱检测。载气为高纯氦气,载气流速1.0 mL·min-1。程序升温:15℃·min-1,60~170℃;5℃·min-1,170305℃;305℃维持6~7 min。进样口的温度为260℃,EI源温度为230℃,电压为70 V。质量扫描范围:m/z 55~800,延迟12 min开始采集,采集速度为20谱·s-1[26-28]。
标准方程建立:分别吸取不同体积的混标A、B、内标溶液(表 1),装入衍生化小瓶中,3个平行,放入快速离心干燥仪中挥干。挥干后的标品用两步法进行衍生化,进行GC-MS分析。标准工作液中色素的质谱响应强度=色素特征碎片质谱响应强度/内标特征碎片质谱响应强度;以加入色素量作为自变量 x ,质谱响应强度作为因变量 y ,求取 x 和 y 的函数关系。
μL 系列浓度混标 Serial number A混标溶液
Mixed standard solution of AB混标溶液
Mixed standard solution of B内标 Internal Standard (L-2-cl-phe, 0.03 mg·L-1) 1 200 200 40 2 100 100 40 3 50 50 40 4 20 20 40 5 10 10 40 6 5 5 40 7 2 2 40 Table 1. Different concentrations of standard-mix solution
-
60.0 mg沙棘浆果加入960.0 μL的冷甲醇-水(3:1,v/v)和40 μL的内标(L-2-氯-苯丙氨酸,0.03 mg·mL-1,甲醇配置),匀浆(Tissuelyser-192,上海净信科技公司),超声提取30 min,低温离心10 min(14 000 rpm,4℃),取700.0 μL的上清液,装入玻璃衍生瓶中,用快速离心浓缩仪挥干后,向玻璃衍生小瓶中加入80.0 μL的甲氧胺盐酸吡啶溶液(15 mg·mL-1),涡旋震荡2 min后,于震荡培养箱中37℃肟化反应90 min,取出后再加入80.0 μL的BSTFA(含1%TMCS)衍生试剂,涡旋震荡2 min后,于70℃反应60 min。取出样本,室温放置30 min,进行GC-MS分析[26-28]。
-
取1.5 g沙棘果实,匀浆,分装于20个1.5 mL离心管中,每管60.0 mg,采用样品加标准品的方式进行方法学考察,加标是采用低(混标6)、中(混标4)、高(混标2)3种加标量(表 1),作为本底的样本不加标,每种样品5个平行。按照“1.2.2 ”中描述的前处理方法进行处理,并进行GC-MS分析。加标液的质谱响应强度=(加标样本的质谱响应强度-本底的质谱响应强度)/内标的质谱响应强度。将加标液的质谱响应强度代入标曲的方程中可以得到计算的标准品量;准确度=标准品计算值/实际加入量×100%[26-28]。
-
H2O2/Fe2+通过Fenton反应产生羟自由基,将邻二氮菲-Fe2+水溶液中Fe2+氧化为Fe3+,导致536 nm吸光度下降, 样品对536 nm吸光度下降速率的抑制程度,反映了样品清除羟自由基的能力,采用羟自由基清除能力检测试剂盒(BC1325, 北京索莱宝科技公司)对羟自由基清除能力进行测定。
-
运用Excel 2013整理数据及作图,采用SPASS 17.0软件分析得到酚类物质定量标准方程,利用单因素方差分析判断果实不同发育时期酚类物质含量和羟自由基清除能力的差异,用相关分析方法分析酚类物质含量与羟自由基清除能力之间的相关关系。
1.1. 试验材料
1.2. 实验方法
1.2.1. 定量方法建立
1.2.2. 沙棘样品前处理
1.2.3. 方法学考察
1.2.4. 羟自由基清除能力测定
1.2.5. 数据统计处理
-
本实验利用芦丁、槲皮素、异鼠李素、山奈酚、杨梅素、柚皮素和维生素E 7种标准品,配制系列混标溶液(表 1),衍生化处理后,进行GC-MS分析。得到相应物质保留时间及特征碎片离子后,选出特异性好且丰度高的特征碎片离子作为此物质定量离子(表 2)。根据定量离子建立标准曲线用于样品中相应物质定量分析,其中,标准工作液中标定物的质谱响应强度=标定物特征碎片质谱响应强度/内标特征碎片质谱响应强度;以加入标定物量作为自变量 x ,质谱响应强度作为因变量 y ,绘制工作曲线并拟合得到标准方程(表 3)。
名称
Compound保留时间
Retention time/min特征碎片离子
Characteristic fragment ion定量离子
Quant massL-2-cl-苯丙氨酸 (2-cl-phe) 12.39 218, 147, 125, 100, 89 218 芦丁 (Rutin) 22.00 217, 204, 175, 147, 129 217 柚皮素 (Naringenin) 29.76 545, 532, 459, 219, 147 545 山萘酚 (Kaempferol) 31.80 559, 487, 272, 193, 147 559 槲皮素 (Quercetin) 32.68 647, 559, 487, 193, 147 647 维生素E (Vitamin E) 32.60 502, 277, 237, 221, 208 237 杨梅素 (Myricetin) 32.85 735, 647, 393, 207, 147 735 异鼠李素 (Isorhamnetin) 33.80 589, 559, 515, 279, 207 589 Table 2. Quantitative information of standard substrates
色素名称
Compound保留时间
Retention time/min定量碎片
Quantmass线性范围
Range/μg方程
Equation相关性系数 R2 检测限
LOD/μg芦丁 (Rutin) 22.00 332 1.250~50.000 y = 0.009 x + 0.006 8 0.997 2 0.250 柚皮素 (Naringenin) 29.76 217 0.050~5.000 y = 0.005 7 x - 0.000 7 0.995 2 0.010 山萘酚 (Kaempferol) 31.80 545 0.005~0.200 y = 0.140 7 x - 0.000 6 0.998 5 0.001 槲皮素 (Quercetin) 32.68 559 0.250~10.000 y = 0.012 2 x - 0.004 0.996 6 0.050 维生素E (Vitamin E) 32.60 647 0.500~50.000 y = 0.031 5 x - 0.034 0.991 4 0.100 杨梅素 (Myricetin) 32.85 237 0.025~1.000 y = 0.036 6 x - 0.000 4 0.999 8 0.005 异鼠李素 (Isorhamnetin) 33.80 735 0.063~2.500 y = 0.037 4 x - 0.002 0.999 0 0.012 Table 3. Establishiment of standard equation
-
以低、中、高3个加标水平考察定量方法的准确度和精密度。3种不同添加浓度水平下考察的准确度为91.36%~109.13%;日内精密度和日间精密度的相对标准偏差(RSD)均小于10%(表 4)。结果显示:整个定量方法准确、稳定、可靠。
物质名称
Compound加标量
Spiked/μg检测量
Observed/μg准确度/%
Accuracy ( n = 5)精密度 RSD/% 日内 (Intra-day, n = 5) 日间 (Inter-day, n = 5) 芦丁(Rutin) 25.000 23.307±1.209 93.23±3.67 5.44 5.45 5.000 5.161±0.436 103.21±7.89 9.09 9.31 1.250 1.240±0.967 99.21±6.32 3.37 4.91 柚皮素(Naringenin) 2.500 2.357±0.023 94.30±8.98 2.91 5.40 0.500 0.517±0.057 103.57±7.56 4.63 7.34 0.125 0.115±0.008 92.38±7.35 3.46 3.40 山萘酚(Kaempferol) 0.100 0.104±0.009 104.23±3.22 2.13 4.79 0.020 0.020±0.008 101.29±3.56 1.34 2.02 0.005 0.005±0.001 107.58±4.12 7.71 8.40 槲皮素(Quercetin) 5.000 4.777±0.345 95.54±7.34 3.10 5.62 1.000 1.037±0.124 103.79±4.67 4.67 5.84 0.250 0.228±0.012 91.36±5.67 2.20 4.53 维生素E(Vitamin E) 25.000 25.817±1.318 103.27±2.12 1.29 3.93 5.000 5.033±0.476 100.67±7.67 3.29 5.93 1.250 1.231±0.114 98.54±8.26 5.54 7.13 杨梅素(Myricetin) 0.500 0.489±0.013 97.90±1.90 2.18 4.38 0.100 0.106±0.012 106.58±7.34 5.03 6.94 0.025 0.027±0.017 109.13±8.67 9.19 9.04 异鼠李素(Isorhamnetin) 1.250 1.235±0.011 98.80±4.67 2.49 4.96 0.250 0.261±0.012 104.54±3.89 2.24 3.94 0.063 0.064±0.004 102.34±6.89 7.53 7.75 Table 4. Results of seven phenolic substrate with relative standard deviation and accuracy
-
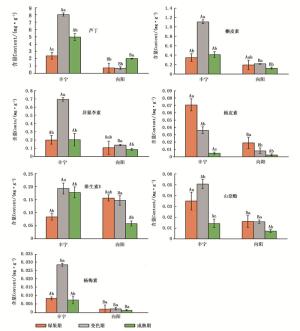
本研究中选择对丰宁和向阳2品种绿果期、变色期和成熟期3个时期沙棘果实的7种酚类物质含量进行测定。在沙棘2品种果实中,芦丁、杨梅素、槲皮素、异鼠李素、柚皮素、山奈酚这6种酚类物质含量在3个时期中丰宁均高于向阳,维生素E含量在变色期和成熟期丰宁高于向阳,其中,在绿果期,芦丁、杨梅素、柚皮素、山奈酚含量差异显著( P <0.05);在变色期,7种酚类物质含量均差异显著( P <0.05);在成熟期,芦丁、杨梅素、槲皮素含量差异显著( P <0.05)。在沙棘果实不同发育时期7种酚类物质含量变化明显,对丰宁7种酚类物质含量分析显示:从绿果期到变色期芦丁、槲皮素、异鼠李素、维生素E、山奈酚和杨梅素6种酚类物质含量显著升高( P <0.05),柚皮素含量显著降低( P <0.05);从变色期到成熟期7种酚类物质含量均显著降低( P <0.05)。对向阳7种酚类物质含量分析显示:从绿果期到变色期槲皮素、异鼠李素、杨梅素3种酚类物质含量升高但差异不显著,芦丁、柚皮素、维生素E、山奈酚4种酚类物质含量降低且柚皮素含量有显著变化( P <0.05);从变色期到成熟期芦丁含量显著升高( P <0.05),槲皮素、异鼠李素、柚皮素、维生素E、山奈酚、杨梅素6种物质含量降低,其中,芦丁、槲皮素、异鼠李素、维生素E、山奈酚含量具有显著变化( P <0.05)(图 1)。
-
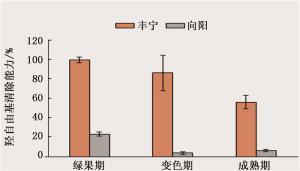
2种沙棘品种间的羟自由基清除能力差异明显。在绿果期,沙棘品种丰宁的羟自由基清除能力是沙棘品种向阳的4倍;在变色期,沙棘品种丰宁的羟自由基清除能力为沙棘品种向阳的23倍;在成熟期沙棘品种丰宁的羟自由基清除能力是沙棘向阳的9倍。由图 2可知:在沙棘品种丰宁中,绿果期的羟自由基清除能力最强,其次为变色期,成熟期最弱;在沙棘品种向阳中,绿果期的羟自由基清除能力最强,其次为成熟期,变色期最弱。
-
将羟自由基清除能力与芦丁、槲皮素、异鼠李素、山奈酚、杨梅素、柚皮素和维生素E这7种酚类物质含量进行相关性分析,结果(表 5)显示:除维生素E外,其它6种酚类物质(芦丁、槲皮素、异鼠李素、山奈酚、杨梅素、柚皮素)与羟自由基的清除能力具有极显著正相关关系( r >0.6, P <0.01)。
羟自由基清除能力 SA/% 芦丁
Rutin槲皮素
Quercetin异鼠李素
Isorhamnetin山奈酚
Kaempferol杨梅素
Myricetin柚皮素
Naringenin维生素
EVitamin E羟自由基清除能力 SA/% 1.000 — — — — — — — 芦丁 (Rutin) 0.611** 1.000 — — — — — — 槲皮素 (Quercetin) 0.663** 0.905** 1.000 — — — — — 异鼠李素 (Isorhamnetin) 0.628** 0.874** 0.990** 1.000 — — — — 山奈酚 (Kaempferol) 0.763** 0.686** 0.853** 0.851** 1.000 — — — 杨梅素 (Myricetin) 0.663** 0.902** 0.965** 0.950** 0.875** 1.000 — — 柚皮素 (Naringenin) 0.768** 0.168 0.312 0.308 0.657** 0.377 1.000 — 维生素E (Vitamin E) 0.170 0.516* 0.581* 0.538* 0.392 0.493* -0.152 1.000 注:*在0.05水平(双侧)上显著相关,* *在0.01水平(双侧)上显著相关。
Notes: *Indicates significant differences at 0.05 level, * * Indicates significant differences at 0.01 level.Table 5. Correlations for seven phenolic compounds related to hydroxyl radical scavenging capacity in seabucthorn fruit
2.1. 待测物定量信息及标准方程建立
2.2. 方法学考察结果
2.3. 沙棘果实发育过程中7种酚类物质的变化规律
2.4. 沙棘果实发育过程中羟自由基清除能力变化规律
2.5. 沙棘果实羟自由基清除能力与7种酚类物质关系
-
果实的羟自由基清除能力(抗氧化能力)是影响果实品质的一个重要因素。对石榴、李、猕猴桃( Actinidia Lindl.)、杏等植物果实的抗氧化能力研究结果显示:羟自由基清除能力与酚类物质的含量呈显著的正相关[8, 9, 30-31]。本研究表明:沙棘中芦丁、槲皮素、异鼠李素、山奈酚、杨梅素、柚皮素这6种酚类物质与羟自由基清除能力呈极显著正相关( r >0.6, P <0.01),与石榴、李、猕猴桃等植物的研究结果一致。因此,芦丁、槲皮素、异鼠李素、山奈酚、杨梅素和柚皮素这6种酚类物质的含量可以为沙棘果实的质量评价提供参考。
选择对沙棘果实3个不同时期进行研究,比之柑橘、猕猴桃、杏、树莓( Rubus idaeus Linn.)中仅选择成熟期进行研究,更能反应在发育过程中酚类物质与羟自由基清除能力之间的关系;但在本研究中选择的沙棘品种数比之柑橘、猕猴桃、杏、树莓有所不足[12, 29-32]。因此,为了更好的对沙棘优良品种的选择提供参考,尚需选择更多沙棘品种做进一步的研究。
尽管本研究中仅对沙棘果实羟自由基清除能力与部分酚类物质含量之间的相关性关系进行了分析,然而果实中除这些酚类物质外,提取物中的其他成分如类胡萝卜素类、维生素类、生物碱类以及原花青素、单宁等物质,也可能共同参与了羟自由基的清除,而这些物质与羟自由基清除能力之间的关系,尚需进一步的研究[30-33]。同时,本研究仅从生理角度探讨了沙棘果中酚类物质与羟自由基清除能力之间的关系,并未深入到其分子调控,因此,在接下来的工作中需要从沙棘转录水平、代谢水平等多个分子层面对沙棘的抗氧化能力进行研究。
-
沙棘中芦丁、槲皮素、异鼠李素、山奈酚、杨梅素、柚皮素这6种酚类物质与抗氧化能力具有极显著正相关性( r >0.6, P <0.01),其含量可以为沙棘果实质量的评价提供参考。





 DownLoad:
DownLoad:
