-
Wright等[1]在2004年首次提出了“叶经济谱”(leaf economics spectrum,LES)的概念,并在全球尺度上定量分析了植物叶片的化学性状(如含氮量、含磷量)、结构性状(如比叶质量)、生理性状(如光合能力、暗呼吸速率)、叶寿命等性状,总结出了它们之间的变化规律和相互关系,并指出叶经济谱是在叶片水平上一系列连续变化的、有规律的生长权衡策略,即在叶经济谱回报慢的一端是叶寿命长、比叶质量大、光合能力弱、暗呼吸速率慢、叶氮和磷含量偏低的“缓慢投资-收益”型物种,另一端则是叶寿命短、比叶质量小、光合能力强、暗呼吸速率快、叶氮和磷含量偏高的“快速投资-收益”型物种[1-4]。因此,叶片的寿命、结构、生理、化学等性状也被称为“叶性状”(leaf traits)[5]。目前,LES的理论和方法已被用于研究分析植物功能性状与环境关系[6]、植物凋落物分解能力[7]、群落构建机制[8]、气候变化[9]、生物多样性[10]等方面,但关于在氮添加条件下植物竞争导致叶性状变化的有关机理研究还较少。
氮沉降是世界性的环境问题,我国已成为继欧洲、北美之后的第三大氮沉降区[11],全国年均氮沉降通量从1980 s的13.2 kg·hm−2增加到2000 s的21.1 kg·hm−2[12]。高浓度的大气氮沉降加上由于土壤施肥引起的外源氮输入,必定会进一步增加植物体内的氮输入量。在我国氮添加最严重的南方区域,栽培最广的用材树种——杉木(Cunninghamia lanceolata (Lamb.) Hook),正遭受着纯林栽培导致的林分地力衰退、生产力下降以及生态环境恶化等一系列问题[13],因此杉木与各种南方阔叶树种的混交栽培研究,以及氮添加条件下的杉木林生长和对环境变化的响应研究受到了科研工作者的广泛关注。叶片对环境的敏感性很强,它通常会通过对自身资源的合理配置和平衡,来减小环境的不利影响。所以,叶片性状的变化能较为准确地反应植株应对环境变化的机理。呼吸作用、光合作用和比叶质量是3个重要的反映植物对资源的投资、利用、回报的叶经济功能性状指标[14]。比叶质量在叶性状研究中使用频率最高,与植物获取资源、潜在生长率和叶片寿命相关性较强[15],在某种意义上反映了叶片吸收资源的效率和能力以及自我保护能力。光合作用和呼吸作用是植物生长代谢的生理基础,光合器官和呼吸器官是叶片的敏感部位[16-17],氮添加能直接影响光合和呼吸机构的性能,从而影响植物的产量。通过了解光合和呼吸的变化,我们可以更好地看出植物对环境变化的自我调节和生长策略。浙江楠(Phoebe chekiangensis C. B. Shang)为我国特有珍稀树种,它不仅是组成常绿阔叶林的主要树种,也是驰名中外的珍贵用材树种[13],它具有耐庇荫,林下枯枝落叶丰富,能提高土壤肥力等特点。因此,本研究主要目的是通过探索单栽杉木幼苗、单栽楠木幼苗以及混栽杉木-楠木幼苗对氮添加的生理适应机制差异,为区域植被恢复,特别是针改阔工程提供支撑。
HTML
-
试验地位于浙江临安浙江农林大学东湖校区(30°16' N,119°44' E),属于中亚热带季风气候区,气候温暖湿润,光照充足。该地区年降水日约158 d,多集中在春夏两季,年降水量达1 454 mm,年平均气温为16.6 ℃,年日照总时长1 826 h,无霜期历年平均237 d,土壤为红黄壤[18]。
-
供试杉木幼苗为来自福建省南平市顺昌洋口国有林场的1年生无性系扦插苗,品种为“洋061”,楠木幼苗为自行栽培的1年生实生苗。杉木幼苗和楠木幼苗的平均地径都为0.5 cm,平均苗高都为30.0 cm。开展试验前进行土壤理化性质测定,结果见表1。
土壤理化性质Physical and
chemical properties of soil全氮Total
N/(g·kg−1)全磷Total
P/(g·kg−1)全钾Total
K/(g·kg−1)速效氮Available
N/(mg·kg−1)速效磷Available
P/(mg·kg−1)速效钾Available
K/(mg·kg−1)pH 数值 Data 1.10 0.311 11.6 80.2 35.6 169 5.26 Table 1. Physical and chemical properties of the experimental soil
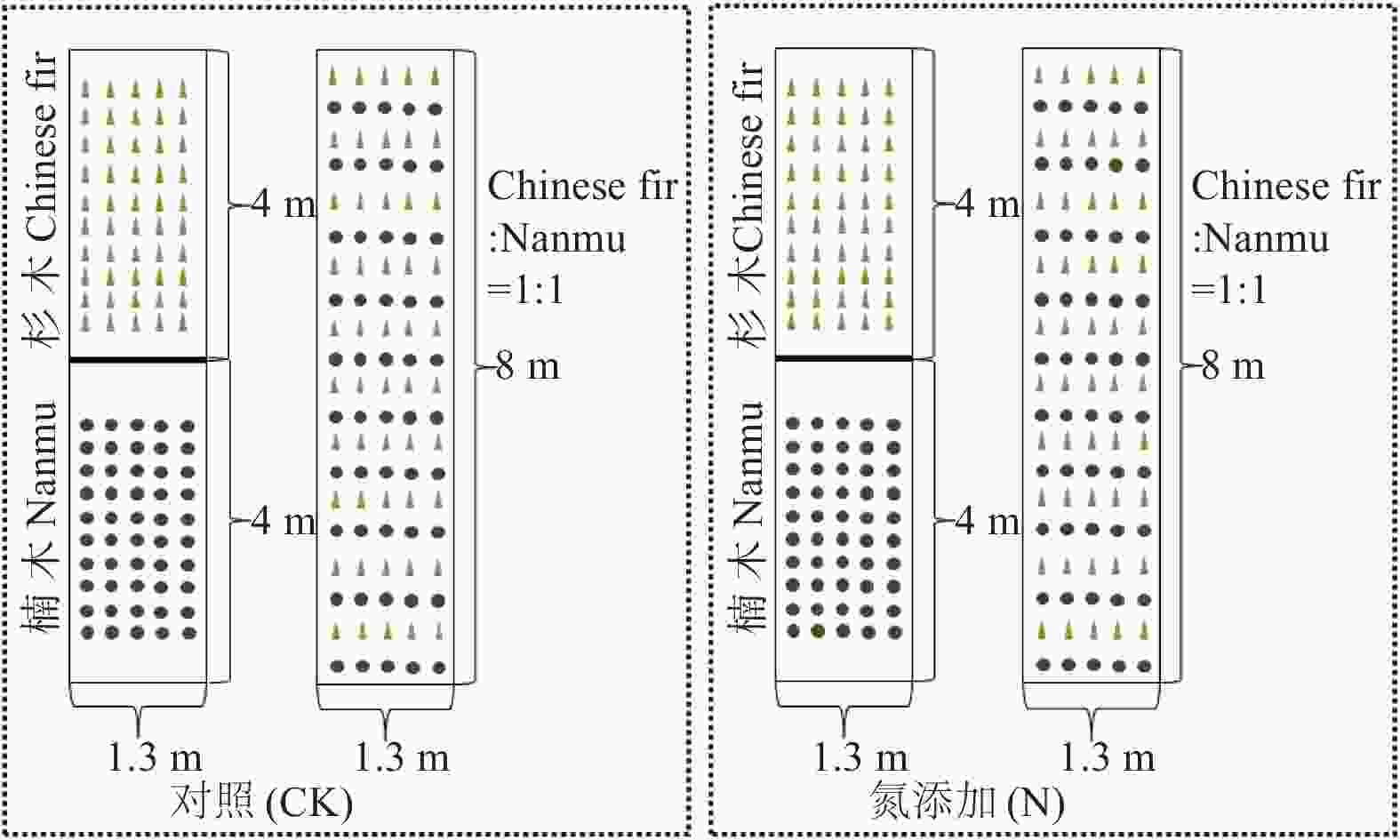
根据临安当地环境氮沉降30 kg·hm−2·a−1的情况[19],试验中的施氮处理为30 kg·hm−2·a−1纯N,幼苗栽植方式包括单栽杉木幼苗、单栽楠木幼苗及其1∶1混栽杉木-楠木幼苗3种方式。本试验共包含2个氮处理,3种栽植方式,其中单栽杉木幼苗和单栽楠木幼苗各有5个重复(两行为1个重复,下同),每个重复包括10个幼苗小重复,混栽幼苗为10个重复,每个重复包括5个杉木幼苗小重复和5个楠木幼苗小重复,杉木幼苗和楠木幼苗各使用200 株。选取健康且长势基本一致的幼苗,种入相应的苗床,植株间距设为30 cm,即种植密度为30 cm·株-1。缓苗1个月后进行施氮处理。苗床8 m×1.3 m共4个,其中两个苗床用木板在4 m处隔断又分为4个小苗床,同一苗床的两个小苗床内分别单栽杉木幼苗和单栽楠木幼苗,另外两个苗床不做处理,用于混栽杉木和楠木幼苗(图1)。
外源氮由NH4NO3和蒸馏水配制而成。将每个处理所需喷施的NH4NO3溶解在10 L蒸馏水中(水量以临安市近10年各月平均降水量为准,平均分配到每周,每周2次),以背式喷雾器人工来回均匀喷洒在氮添加组幼苗上,对照组喷洒等量蒸馏水。试验时间为2018年4月至6月。
-
土壤理化性质的测定:随机取每个苗床的5份土样,采用半微量凯氏定氮法测定土壤全氮含量;采用NaOH碱熔-钼锑抗分光光度法测定土壤全磷含量、原子吸收火焰光度计法测定土壤全钾含量;采用碳酸氢钠浸提-钼锑抗分光光度法测定土壤中有效磷含量;采用乙酸铵浸提-原子吸收火焰分光光度计法测定土壤速效钾含量;采用碱解扩散法测定土壤中水解性氮含量;采用玻璃电极法测定土壤pH。
株高(H)、地径(D)和冠幅(W)的测定:每个处理随机选择5株植物,用钢卷尺测量它们的株高(地面到植株主干顶端的高度)与冠幅(植株南北方向和东西方向宽度的平均值),用游标卡尺测定其地径(贴近地面植株主干直径)。
净光合速率(PN)和单位质量最大净光合速率(Amass)的测定:采用便携式光合作用测定系统(LI-6800,LI-COR,美国)进行气体交换参数测定。在晴朗上午的8:00—11:30选择测过生长量的植株的第4片完全展开的叶片进行测定。测定时调节仪器参数,叶室温度26 ℃、光照强度1 600 μmol·m−2·s−1、相对湿度60%、CO2摩尔分数(400±5) μmol·mol−1。测定净光合速率(PN)和单位面积最大净光合速率(Aarea),并计算单位质量最大净光合速率(Amass):Amass=Aarea×SLA(比叶面积)/10 000[20]。
最大光化学量子产量(FV/Fm)的测定:将测光合的叶片经过20 min暗适应,再用调制叶绿素荧光成像仪器(PAM-2500,WALZ,德国)测定最大光化学量子产量(FV/Fm)。
呼吸速率(Rd)的测定:将黑色塑料袋套在上述叶片上,暗适应40 min。采用便携式光合作用测定系统(LI-6800,LI-COR,美国)进行呼吸速率(Rd)的测定。测定时调节仪器参数,叶室温度26 ℃、光照强度0 μmol·m−2·s−1、相对湿度60%、CO2摩尔分数(400±5) μmol·mol−1。
比叶质量(LMA)和比叶面积(SLA)的测定:将测定光合及荧光参数所用叶片采下,放于两张透明膜片之间,然后放置于扫描仪上,采用图像处理软件Image J对叶片图像进行扫描并得出叶面积数据。将测定后的叶片置于85 ℃烘箱中烘干至恒质量,用电子天平(精度为0.000 1 g)称质量。比叶质量(LMA)和比叶面积(SLA)计算公式:LMA(g·cm–2)=叶片干质量(g)/叶面积(cm2)[14],SLA(cm2·g–1)=叶面积(cm2)/叶片干质量(g)。
-
利用SPSS的单因素方差分析法(one-way ANOVA)和Duncan多重比较法对数据进行统计分析,用LSD多重检验法比较叶片的株高、地径、冠幅、净光合速率和呼吸速率等数据在不同处理间的差异显著性。利用三因素方差分析法(three-way ANOVA)对树种、种植方式和氮处理进行三因素方差分析。
1.1. 试验地概况
1.2. 试验材料和设计
1.3. 研究方法
1.4. 数据处理
-
表2表明:在没有施氮状态下,单栽杉木幼苗土壤的速效钾显著高于单栽楠木幼苗土壤17.8%,而单栽杉木幼苗土壤的pH、速效氮和速效磷与单栽楠木幼苗土壤差异不显著,说明单栽楠木幼苗土壤中解钾微生物高于单栽杉木幼苗。混栽幼苗土壤的速效钾显著高于单栽幼苗土壤,但pH、速效氮和速效磷与单栽幼苗土壤没有显著差异。
施氮后,单栽杉木幼苗土壤的速效氮、速效磷和速效钾分别比单栽楠木幼苗土壤显著高18.7%、31.2%和17.8%,但是pH与单栽楠木幼苗土壤没有显著差异。单栽杉木幼苗土壤的pH和速效磷与对照没有显著差异,但是单栽杉木幼苗土壤的速效氮显著高于对照,而速效钾显著低于对照。单栽楠木幼苗土壤的pH与对照差异不显著,但速效氮显著高于对照,而速效磷和速效钾显著低于对照。由此可见,氮添加能显著增加单栽幼苗土壤的速效氮,同时加快速效钾的流失。
施氮后,混栽林幼苗土壤的pH与单栽幼苗土壤的差异不显著,但是速效氮、速效磷和速效钾显著低于单栽杉木幼苗土壤24.9%、32.1%和18.6%,而与单栽楠木幼苗差异不显著。氮添加显著降低了混栽林幼苗土壤的速效磷,极显著降低了速效钾,可见氮添加能加快混栽林幼苗土壤的速效磷和速效钾的流失,长期的氮添加会抑制植物的生长。
树种
Varieties of trees种植方式
Planting patterns氮处理
Nitrogen disposepH 速效氮
Available N/
(mg·kg−1)速效磷
Available P/
(mg·kg−1)速效钾
Available K/
(mg·kg−1)杉木幼苗
Chinese fir seedlings单栽
Pure plantation+ 5.27±0.500a 55.0±2.52a 41.7±2.12a 153±1.21c − 5.81±0.212a 41.5±1.93bc 44.7±1.34a 172±1.29b 楠木幼苗
Nanmu seedlings单栽
Pure plantation+ 5.75±0.238a 46.3±1.61b 31.8±2.08b 130±2.59d − 5.98±0.280a 37.6±1.66c 40.7±2.10a 146±2.94c 杉木-楠木幼苗
Chinese fir and nanmu seedlings混栽
Mixed plantation+ 5.43±0.390a 41.3±2.08bc 28.3±1.22b 124±4.18d − 5.71±0.370a 39.4±2.70c 39.2±2.47a 185±2.63a 注:图中不同字母表示杉木幼苗与楠木幼苗之间的差异性显著(P<0.05)。“+”表示添加氮,“-”表示未添加氮。下同。
Note: Small letters indicate significant differences between Chinese fir seedlings and nanmu seedlings(P<0.05). “+” indicates nitrogen addition, and “-” indicates no nitrogen addition. The same meanings in the following tables.Table 2. Physical and chemical properties of the soil of Chinese fir seedlings and nanmu seedlings
-
在没有施氮条件下,单栽杉木幼苗和楠木幼苗的H、D和FV/Fm并没有存在显著差异,但是杉木的W比楠木低31.2%,差异显著(表3)。
树种
Varieties of trees种植方式
Planting patterns氮处理
Nitrogen dispose株高
Plant
height/cm地径
Ground
diameter/cm冠幅
Crown
width/cm最大光化学量子产量
Maximum photochemical
quantum yield杉木幼苗
Chinese fir seedlings单栽
Pure plantation+ 41.3±1.46b 0.704±0.032a 24.8±1.25b 0.789±0.002a − 41.0±1.62b 0.658±0.027ab 24.5±1.70b 0.743±0.021ab 混栽
Mixed plantation+ 38.7±0.95b 0.646±0.016ab 22.9±0.77b 0.781±0.005ab − 39.7±1.37b 0.644±0.019ab 24.5±0.87b 0.777±0.014ab 楠木幼苗
Nanmu seedlings单栽
Pure plantation+ 45.1±1.69a 0.523±0.014b 37.8±1.26a 0.750±0.004ab − 37.7±1.00b 0.532±0.014b 35.6±0.76a 0.735±0.012b 混栽
Mixed plantation+ 42.4±1.30ab 0.591±0.016b 38.5±1.00a 0.718±0.036b − 45.7±1.26a 0.598±0.018b 38.2±0.96a 0.734±0.016b Table 3. The increment and leaf physiological traits of Chinese fir seedlings and nanmu seedlings
在混栽状态下,杉木幼苗的D和FV/Fm与楠木幼苗没有显著差异,但是杉木的H和W分别显著比楠木低13.3%和35.7%。另外,混栽杉木幼苗的H、D、W和FV/Fm与单栽杉木幼苗差异不显著。混栽楠木幼苗的D、W和FV/Fm与单栽楠木幼苗的差异并不显著,但是H显著升高,比单栽幼苗高21.2%。
施氮后,单栽杉木幼苗的H、D、W和FV/Fm与对照相比没有显著变化。单栽楠木幼苗的D、W和FV/Fm与对照相比没有显著变化,但是H显著增加了19.6%。且单栽杉木幼苗的FV/Fm与单栽楠木幼苗没有显著差异,但单栽杉木幼苗的D显著高于单栽楠木幼苗,而单栽杉木幼苗的H和W显著低于单栽楠木幼苗。
施氮后,混栽杉木幼苗和混栽楠木幼苗的H、D、W和FV/Fm与各自对照相比都没有显著变化。混栽杉木幼苗的H、D和FV/Fm与混栽楠木幼苗没有显著差异,但混栽楠木幼苗的W显著高于杉木幼苗67.8%。
-
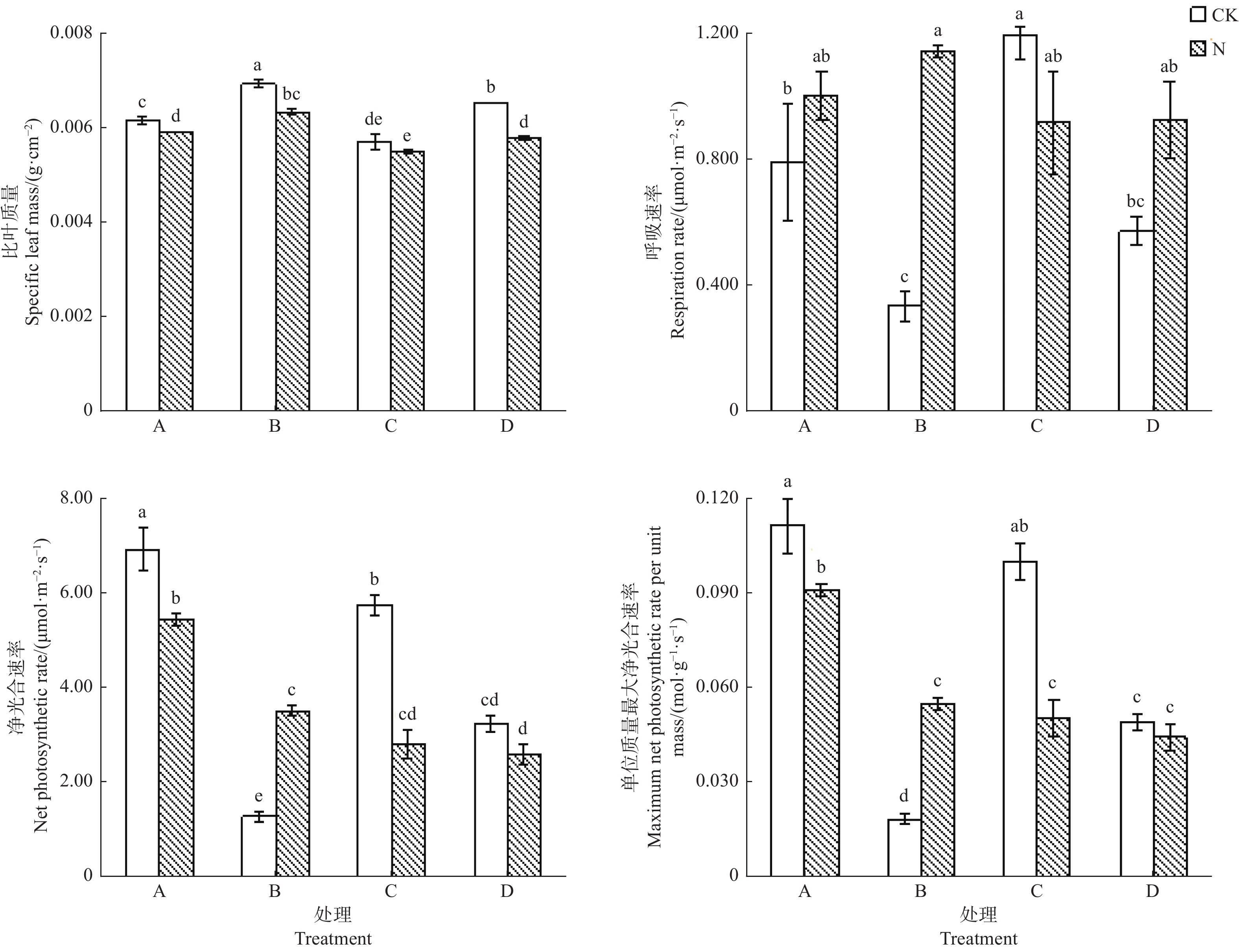
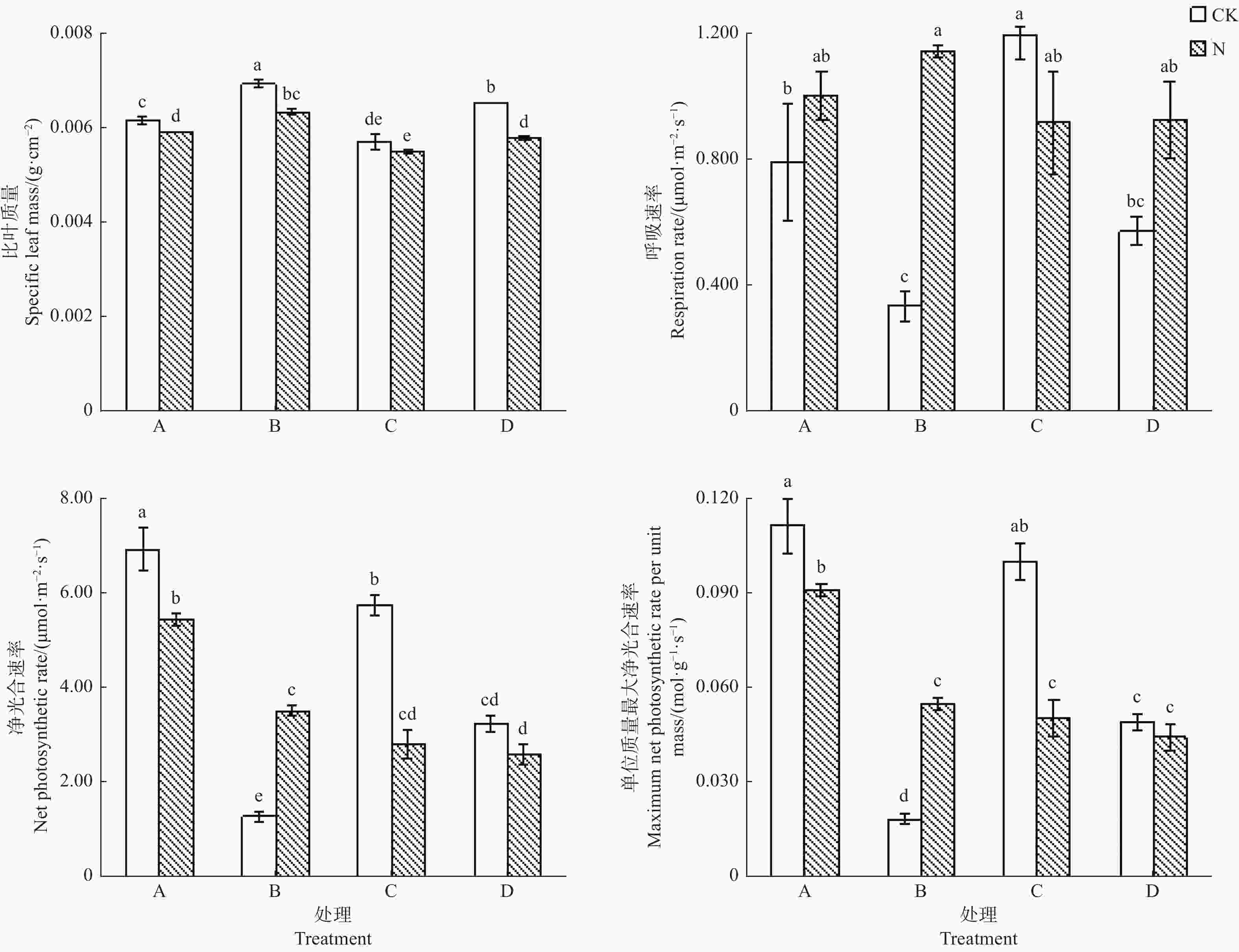
在没有施氮状态下,单栽杉木幼苗的Rd、PN和Amass分别显著高于单栽楠木幼苗132%、436% 和450%,而单栽杉木幼苗的LMA显著低于单栽楠木幼苗14.3%,可见杉木幼苗通过减小叶片厚度和叶肉细胞密度[17],来增加叶片的呼吸速率和光合速率(图2)。
在没有施氮状态下,混栽杉木幼苗的Rd、PN和Amass显著高于混栽楠木幼苗,而混栽杉木幼苗的LMA比混栽楠木幼苗显著低12.3%,与单栽幼苗状态基本一致。混栽杉木幼苗的Amass与单栽幼苗相比差异并不显著,但是混栽杉木幼苗的LMA和PN显著低于单栽幼苗,而Rd显著高于单栽幼苗;混栽楠木幼苗的Rd与单栽幼苗相比差异并不显著,但是混栽楠木幼苗的PN和Amass显著高于单栽幼苗,而LMA显著低于单栽幼苗。
施氮后,单栽杉木幼苗的Rd与单栽楠木幼苗差异不显著,但是PN和Amass分别比单栽楠木幼苗显著高54.3%和67.3%,而LMA比单栽楠木幼苗显著低7.8%。单栽杉木幼苗的Rd与对照没有显著差异,但是单栽杉木幼苗的LMA、PN和Amass显著高于对照。单栽楠木幼苗的Rd和PN极显著高于对照,Amass显著高于对照,但是LMA显著低于对照。由此可见,氮添加对楠木幼苗叶性状的影响大于杉木幼苗的影响。
施氮后,混栽杉木幼苗的Rd、PN和Amass与混栽楠木幼苗差异不显著,但是LMA比混栽楠木幼苗显著低5.2%。氮添加显著降低了混栽杉木幼苗的PN和Amass,分别比无氮添加低51.1%和49.5%,但是对LMA和Rd没有显著影响。施氮对混栽楠木幼苗PN和Amass的影响不显著,但是显著提高了Rd,显著降低了LMA。
-
由表4可以看出,树种对叶片的H、D、W、FV/Fm、LMA、Rd、PN和Amass均有显著影响;种植方式对叶片的D、PN和Amass有显著影响;氮添加对叶片的FV/Fm、LMA、Rd和Amass有显著影响;树种和氮添加的交互作用对叶片的D、W、FV/Fm、LMA、Rd、PN和Amass有显著影响;种植方式和氮添加的交互作用对叶片的H、Rd、PN和Amass有显著影响。
参数
Parameters树种
Varieties of trees种植方式
Planting patterns氮添加
Nitrogen addition树种×氮添加
Varieties of trees ×
Nitrogen addition种植方式×氮添加
Planting patterns ×
Nitrogen additionF P F P F P F P F P H 16.7* 0.001* 0.30 0.594 1.85 0.192 3.6 0.075 24.00* 0.000* D 270.6* 0.000* 5.89* 0.027* 1.82 0.196 7.3* 0.016* 2.62 0.125 W 825.8* 0.000* 1.16 0.297 0.13 0.724 4.6* 0.047* 3.23 0.091 FV/Fm 2 079.5* 0.000* 0.80 0.385 5.78* 0.029* 23.9* 0.000* 0.59 0.455 LMA 2 033.1* 0.000* 0.72 0.409 5.96* 0.027* 23.7* 0.000* 0.56 0.467 Rd 9.2* 0.008* 1.24 0.281 13.21* 0.002* 16.3* 0.001* 9.60* 0.007* PN 230.2* 0.000* 16.71* 0.001* 17.93* 0.001* 79.1* 0.000* 40.92* 0.000* Amass 237.1* 0.000* 16.94* 0.001* 18.05* 0.001* 78.1* 0.000* 40.40* 0.000* *P<0.05. Table 4. Three-way ANOVA of Chinese fir seedlings leaves and nanmu seedlings leaves
2.1. 氮添加对混栽状态下的杉木幼苗和楠木幼苗土壤理化性质的影响
2.2. 氮添加对混栽状态下的杉木幼苗和楠木幼苗生长量和叶片生理性状的影响
2.3. 氮添加对混栽状态下的杉木幼苗和楠木幼苗叶片结构和功能的影响
2.4. 氮添加与树种、种植方式的交互作用对混栽状态下的杉木幼苗和楠木幼苗叶片的影响
-
Wright等[1]提出的叶经济谱理论阐述了自然界的植物投资由回报快到回报慢、由急进到稳健的连续变异特征,回报快的植物具有低比叶质量、高光合和呼吸速率,短寿命,高营养含量等特点,回报慢的植物具有高比叶质量、低光合和呼吸速率,长寿命,低营养含量等特点[21-22]。叶片是植物暴露在环境中面积最大的器官,其结构和功能的变化必然影响到整株植物的生长代谢过程。植物的性状对其生活对策和竞争能力起到决定性作用,其中对竞争贡献较大的是叶片结构性状(如比叶质量)和生理性状(如光合速率)[2]。当环境发生改变时,植物将通过改变比叶质量、光合能力和呼吸速率等自身叶性状来改变生活策略,对资源利用进行重新分配,使得自己在不利环境条件下更具有竞争力。
本研究发现在无氮添加条件下,单栽杉木幼苗的比叶质量显著低于单栽楠木幼苗,但是杉木幼苗的光合能力和呼吸速率显著高于楠木幼苗,根据Reich[14]的研究可以推测,在幼苗期间,杉木更靠近叶经济谱回报快(急进)的一端,而楠木更靠近回报慢(稳健)的一端,杉木幼苗生长速度大于楠木。这可能是因为叶片在功能效率和结构建成两个方面有着“此消彼长”的资源权衡策略,由于在有限的资源环境下,植物一方面的资源投入多,另一方面投入就要减少[23]。本试验表明杉木幼苗较低的比叶质量说明它有较大的叶面积,能够增加光的获取量,因此杉木幼苗的光合能力要高于楠木幼苗。混栽杉木幼苗的单位质量最大净光合速率与单栽幼苗相比差异并不显著,但是混栽杉木的比叶质量和净光合速率显著低于单栽幼苗,而呼吸速率显著高于单栽幼苗,这与刘明秀[24]等人发现植物比叶质量和净光合速率呈负相关的研究结果相反,他们认为比叶质量大的植物,细胞壁厚,叶肉细胞导度低,CO2的同化速率低,最终导致叶片光合能力降低。本试验出现相反结果的原因可能是,楠木幼苗的株高和冠幅显著大于杉木幼苗,楠木的枝条和叶片遮挡了部分杉木叶片的光照,使得杉木叶片对光的吸收量减少,以致净光合速率降低。混栽楠木幼苗的呼吸速率与单栽幼苗相比差异并不显著,但是混栽楠木幼苗的光合能力显著高于单栽幼苗,而比叶质量显著低于单栽幼苗。Mao[25]等人的研究表明,土壤中速效氮含量较高,植物能够吸收较多的土壤肥力用于合成叶片细胞和与光合作用有关的酶,从而提高光合速率,这与本试验结果一致。杉木幼苗和楠木幼苗混栽可能会使树种的生态位重叠,即两个树种在其与生态因子联系上的相似性[26],这使得楠木能够更加充分地利用环境资源。本试验结果表明,在混栽情况下,楠木幼苗处于上层,杉木幼苗处于下层,混栽楠木幼苗的株高、地径、冠幅大于单栽楠木幼苗,而混栽杉木幼苗的株高和地径小于单栽杉木幼苗,两者为争夺有限的资源产生了种间竞争[27-28],两者都把更多的能量分配到了竞争之中,它们通过增大比叶面积来增加光和其他资源的获取量来同化器官,提高叶片资源利用率,加强自身的竞争能力,但楠木幼苗的竞争能力更强。另一方面,混栽状态改变了楠木幼苗的叶性状,使得楠木幼苗更靠近叶经济谱回报快的一端,但混栽状态不改变杉木幼苗的生长策略。
施氮显著增加了单栽杉木幼苗的比叶质量和光合能力,对呼吸速率的影响不显著。但是施氮极显著增加了单栽楠木幼苗的呼吸速率和光合能力,而显著降低了单栽楠木幼苗的比叶质量。氮添加在一定程度上提高楠木幼苗的光合能力,使得叶片中的光合产物较多,这样幼苗具有丰富的光合产物,从而提高了呼吸速率,这与前人的很多研究结果[29]都一致。由此可见,氮添加对不同树种的影响不同。氮添加促使楠木幼苗向叶经济谱回报快的一端发展,即更趋向于叶寿命短、比叶质量小、光合能力强、暗呼吸速率快、叶氮和磷含量偏高的“快速投资-收益”的生长策略;而单栽杉木在施氮情况下选择保守性的生长策略,资源获取能力降低,生长缓慢。因此得出,叶片具有很强的可塑性[30],植物能够通过改变叶片的结构和功能来适应环境的变化。与没有施氮的混栽杉木-楠木幼苗相比,施氮的混栽杉木幼苗光合能力显著降低;施氮的混栽楠木幼苗呼吸速率显著升高,但比叶质量显著降低。由于氮添加显著降低了混栽林幼苗土壤的速效磷,极显著降低了速效钾,这可能对混栽杉木幼苗生长的不利影响较强,而对楠木幼苗的影响较弱[31],这说明在竞争状态下,杉木幼苗和楠木幼苗对氮添加不同的响应与自身因素有关,杉木对环境的敏感性强于楠木,试验添加的氮含量不足以对楠木幼苗产生影响,这可能是因为楠木幼苗的耐酸性强于杉木幼苗,也有可能是氮添加使得杉木幼苗中与光合相关的酶含量和酶活性降低[32]。氮添加使混栽林杉木幼苗向叶经济谱回报慢的一端发展,而楠木幼苗向叶经济谱回报快的一端发展,这恰好反映了两种不同的生长策略。另外,由于本试验持续时间较短,在氮沉降条件下,杉木和楠木在不同的生长时期所表现出的生长情况可能会有一定差异,这需要较长时期的试验进行研究。
-
综上所述,氮添加和混栽对杉木幼苗和楠木幼苗叶性状的影响显著。在没有施氮的情况下,单栽杉木幼苗更靠近叶经济谱回报快(急进)的一端,而单栽楠木幼苗更靠近回报慢(稳健)的一端,但混栽的种植方式改变了楠木幼苗的叶性状,使得楠木幼苗更靠近叶经济谱回报快的一端,但不改变杉木幼苗的生长策略。而氮添加促使单栽楠木幼苗进一步向叶经济谱回报快的一端发展,但是对杉木幼苗在叶经济谱中的位置影响不大。但是在混栽状态下,氮添加使杉木幼苗向叶经济谱回报慢的一端发展,而楠木幼苗向叶经济谱回报快的一端发展。本研究对于揭示氮添加条件下,植物在幼苗时期叶性状的适应机制具有重要意义。





 DownLoad:
DownLoad: